Kurzzusammenfassung
Prinzipiell kann jede Tumorentität des Bewegungsapparats auch am Fuß zu finden sein. Gutartige Tumoren und tumor-ähnliche Läsionen sind dabei deutlich häufiger anzutreffen, als maligne. Sowohl primäre, maligne Knochen- und Weichteiltumoren wie das Chondrosarkom oder Synovialsarkom als auch Metastasen stellen relevante Differentialdiagnosen unklarer Knochenläsionen und Weichteilformationen dar, die es abzuklären gilt. Eine wesentliche Aufgabe des Fußchirurgen liegt deshalb darin, entsprechende Differentialdiagnosen zu berücksichtigen und die erforderlichen weiterführenden Schritte in Diagnostik und Therapie einzuleiten. Bis auf Ausnahmen ist die Anamnese bei diesen Erkrankungen unspezifisch. Essentieller Bestandteil der bildgebenden Diagnostik unklarer Knochenläsionen ist unverändert die konventionelle Röntgenaufnahme. Hierdurch können wertvolle Informationen bezüglich biologischem Verhalten und Wachstumsgeschwindigkeit gewonnen werden. Charakteristische, manchmal gar pathognomonische Veränderungen in Röntgenbild und MRT erlauben in einigen Fällen die Diagnose und ggf. die direkte Tumorresektion. Häufig bleibt jedoch die Biopsie das einzige Mittel, eine definitive Diagnose histopathologisch zu sichern und somit die Art der operativen Therapie festzulegen. Eine Verzögerung in der spezifischen Diagnostik und Therapie aggressiver Läsionen kann folgenschwere Konsequenzen nach sich ziehen. Im Folgenden werden deshalb die wichtigsten Schritte in Diagnostik und Therapie von Tumoren und tumor-ähnlichen Läsionen des Fußes und Sprunggelenks dargestellt. Dabei muss der Kenntnisvermittlung prinzipieller Grundlagen der Tumororthopädie (z.B. wann und wie biopsiere ich?) in diesem Rahmen ein höherer Stellenwert eingeräumt werden, als detaillierte Behandlungsabläufe einzelner Tumorarten aufzulisten. Die Fülle potentieller Entitäten wäre zu groß.
Besonders relevante und interessante Entitäten werden detailliert diskutiert. Unterschiedliche Möglichkeiten der Tumortherapie werden erörtert und durch spezifische, auf die jeweilige Tumorart bezogene Prozeduren ergänzt.
Definition Tumor und Fußtumor
Prinzipiell kann jede lokalisierte Raumforderung als Tumor bezeichnet werden. Dies beinhaltet im weitesten Sinn auch Schwellungszustände, die beispielsweise auf ein Hämatom oder eine Entzündung zurückzuführen sind. Dementsprechend erlaubt es der Begriff "Tumor" nicht, Aussagen über die Natur und das biologische Verhalten der Raumforderung zu treffen. Im engeren Sinn versteht man unter einem Tumor jedoch eine benigne oder maligne Neoplasie, also Neubildung von Körpergewebe, die durch eine Fehlregulation des Zellwachstums entsteht (autonome, pathologische Gewebevermehrung).
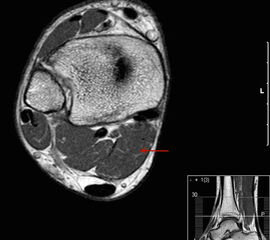
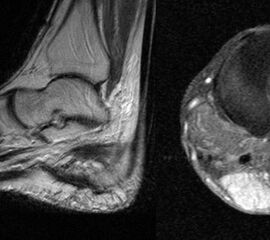
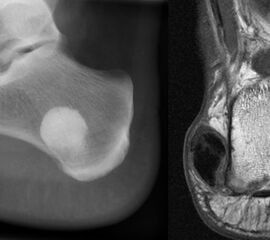
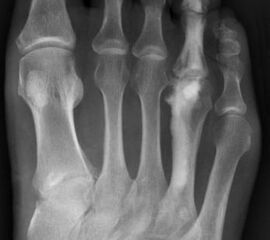
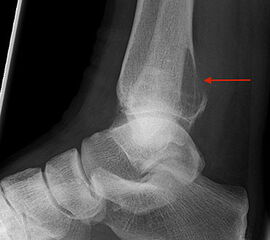
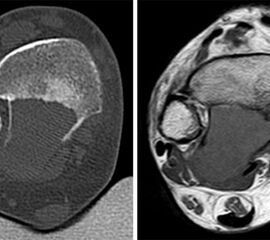
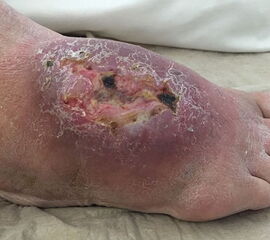
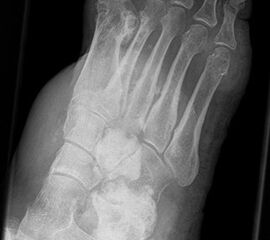
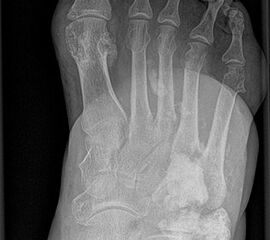
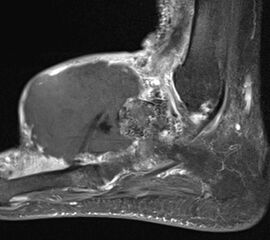
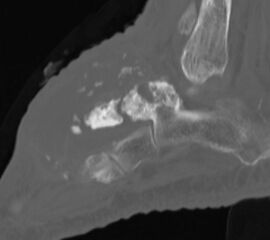
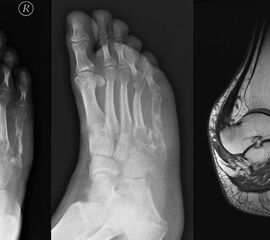
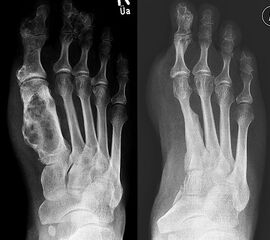
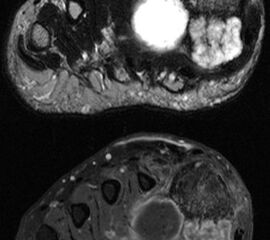
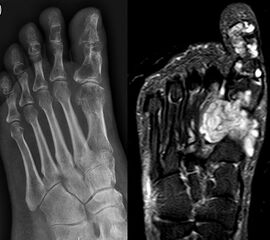
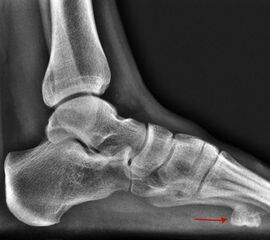
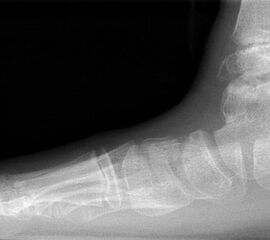
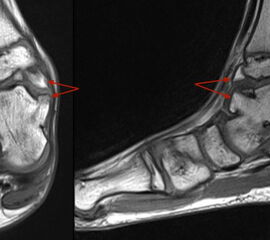
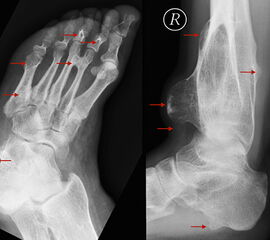
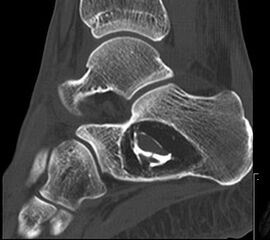
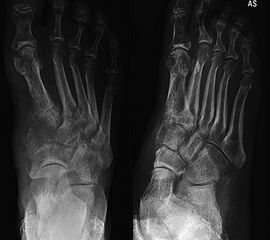
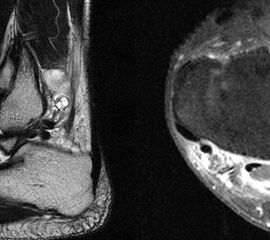
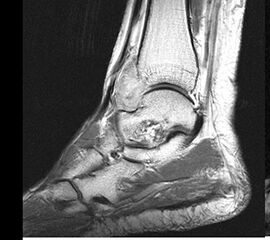
Davon abzugrenzen sind tumor-ähnliche Läsionen (tumor-like lesion) bzw. Pseudotumoren. Eine strikte Differenzierung zwischen diesen beiden Begriffen ist nicht möglich, allgemein gültige Definitionen für diese Begriffe existieren nicht. Generell bieten tumor-ähnliche Läsion und Pseudotumoren zwar den klinischen und zum Teil auch radiologischen Aspekt einer echten Neoplasie, nicht aber das biologische Verhalten. Konkret werden hierzu u.a. Ganglien (intraossär und weichteilig), Fremdkörpergranulome (weichteilig), aber auch akzessorische Muskeln (z.B. M. soleus accessorius, Abb. 1) und Abszessformationen 12 gezählt. Andere Vertreter dieser Art, insbesondere am Fuß lokalisiert, beinhalten u.a. Warzen und Hyperkeratosen aber auch das Morton-Neurom oder die Plantarfibromatose (M.Ledderhose) (Abb. 2). Sehr seltene, aber gehäuft am Fuß zu findende Pseudotumoren beinhalten die Tumoröse Kalzinose 3 und die Melorheostose, die an dieser Stelle nur beispielhaft genannt werden sollen. Die Tumoröse Kalzinose beruht auf einer Störung des Kalzium- und Phosphathaushalts und zeigt eine Prädilektion für mechanisch stark belastete Regionen 4 (Abb. 3). Bei der Melorheostose handelt es sich um eine gutartige Kortikalisverdickung mit unregelmäßigen Hyperostosen entlang einer Extremitat (Abb. 4). Die Ätiologie der auch als Kerzenwachskrankheit bezeichneten, meist monomelischen Veränderung ist unklar (Knöller, 2002).
Die WHO-Klassifikation muskulo-skelettaler Tumoren (Fletcher, 2013) unterscheidet außerdem “Tumours of undefined neoplastic nature“, also Knochenläsionen, die im Allgemeinen als nicht-neoplastisch betrachtet werden, in der Differenzialdiagnose echter Knochentumore aber dringend berücksichtigt werden müssen. Einige besitzen morphologische und zytogenetische Merkmale echter Neoplasien, obwohl das klinische Verhalten eher eine nicht-neoplastische Natur unterstützt. Häufigste Beispiele hierfür sind die juvenile (simple) Knochenzyste und die fibröse Dysplasie.
Ein echter Tumor dagegen ist durch enthemmtes, autonomes und in der Regel irreversibles Überschusswachstums von körpereigenem Gewebe, welches mit unterschiedlich ausgeprägtem Verlust spezifischer Zell- und Gewebefunktionen einhergeht, charakterisiert. Insbesondere im Patientengespräch ist darauf zu achten, die Begrifflichkeiten verständlich zu erklären und nahezubringen, dass die Diagnose eines "Tumors" nicht zwangsweise, sondern nur im seltensten Fall einer Krebserkrankung entspricht.
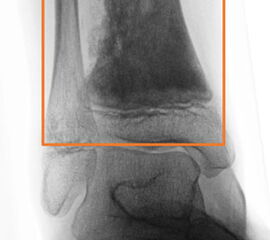
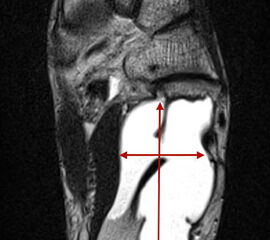
In unserem eigenen Patientengut werden alle gut- und bösartige Knochen- und Weichteiltumoren des Fußes, einschließlich dem Bereich der distalen Metaphyse der Tibia und Fibula als Fußtumoren definiert. Die Metaphyse ist hierbei durch ein gleichseitiges Rechteck (Quadrat) festgelegt (Abb. 5), das seine Basis am breitesten Teil der Wachstumsfuge hat (Ruedi, 2000). Explizit ausgeschlossen hiervon werden alle oben genannten Pseudotumoren.
Epidemiologie und Ätiologie
Epidemiologie
Klinische Nachuntersuchungen zeigen, dass bösartige Neubildungen des Fußes deutlich häufiger sind als allgemein vermutet. Die Fuß- und Sprunggelenksregion, welche ca. 3% der gesamten Körpermasse darstellt, wird korrespondierend in 3–5% aller Fälle von Knochenneubildungen betroffen (Dahlin, 1986)5. Dabei sind Weichteiltumoren im Bereich des Fußes sogar noch häufiger häufig vertreten. 5% aller malignen und 8% aller benignen Weichteiltumoren überhaupt finden sich am Fuß 6. Differenzierte Verteilungsmuster von Fußtumoren bezüglich Dignität und ihres knöchernen oder weichteiligen Ursprungs sind gemäß Nachuntersuchungen verschiedener spezialisierter Tumorzentren jedoch sehr unterschiedlich. Je nach Autor und Krankengut schwankt der Anteil maligner Neoplasien am Fuß zwischen 13 und 39%. Weichteiltumoren machen 25–52% und Knochentumoren 48– 75% aller Fußtumoren aus 578. Das durchschnittliche Alter zum Zeitpunkt der Diagnose liegt zwischen 24 und 30 Jahren (1–84 Jahre). Eine eindeutige geschlechtsspezifische Präferenz besteht in der Zusammenfassung aller Entitäten nicht. Bezüglich Lokalisation sind das Fersenbein und die Metatarsalia die statistisch am häufigsten von Knochentumoren befallenen Fußskelettbereiche. Die bislang bezüglich Fallzahlen größte und aktuellste Übersicht über Fußtumoren wurde im Jahr 2015 von Ruggieri et al. aus dem Rizzoli Institut Bologna veröffentlicht 9: Bei insgesamt 1170 Fußtumoren (Alter der Patienten: 5-81 Jahre) lag der Anteil an Knochentumoren bei 83,8% (n=981) und der von Weichteiltumoren bei 16,2% (n=189). Der Anteil bösartiger Neubildungen lag bei Knochenläsionen bei 20,6% (n=202) und bei Weichteiltumoren bei knapp 52% (n=98).
Diese Angaben decken sich nur zum Teil mit unseren eigenen Daten zu Fußtumoren. Insgesamt 5,5% aller Tumorerkrankungen unseres Patientenkollektivs aus den Jahren 1997 bis 2015 waren im Bereich des Fußes und Sprunggelenks lokalisiert. Pseudotumoren wie Arthrosezysten, Sehnenganglien, das Morton-Neurom oder die Plantarfibromatose wurden von der Erfassung ausgeschlossen. Das durchschnittliche Alter von 409 Patienten mit Fuß- und Sprunggelenkstumoren betrug 45±19 Jahre (min.5, max.96 Jahre), eine geschlechtsspezifische Präferenz bestand nicht. 258 Tumoren betrafen den Knochen (63,1%), darunter 230 gutartige und 28 bösartige (10,8%). Die 151 Weichteiltumoren unseres Kollektivs setzten sich in aus 110 gutartigen und 41 bösartigen (37,3%) Geschwulsten zusammen.
Die häufigsten gutartigen Knochentumoren waren die juvenile Knochenzyste (n=46), das Enchondrom (n=40) und die aneurysmatische Knochenzyste (n=26). Die häufigsten bösartigen Knochentumoren waren das Chondrosarkom (n=13), das Osteosarkom (n=4) und das Ewingsarkom (n=3). Weichteilig fanden sich an gutartigen Geschwülsten am häufigsten Hämangiome (n=17), die PVNS (n=13) und Schwannome (n=8). Bei den gutartigen Weichteiltumoren zeigte sich ein sehr breites Spektrum an Entitäten, so dass nahezu die Hälfte aller Fälle (43%) auf Tumorarten entfiel, die seltener als fünf Mal beobachtet werden konnten. Bösartige Weichteiltumoren setzten sich vornehmlich aus Synovialsarkomen (n=8), dem Melanom (n=7) und NOS-Sarkomen (Syn. Pleomorphe Sarkome, MFH) (n=6) zusammen.
Diese unterschiedlichen Verteilungsmuster zeigen, wie heterogen das Krankheitsbild "Fußtumor" wirklich ist. Eine mögliche Erklärung der uneinheitlichen Statistiken mag sein, dass ein Großteil benigner Knochenläsionen aufgrund fehlender Symptomatik unentdeckt bleibt oder lediglich als Zufallsbefund erscheint 10. Dies zeigen auch die Beobachtungen weiterer großer muskuloskelettaler Tumorzentren (Campanacci, 1999; Wirth, 2004).
Primäre maligne Knochentumoren, also Knochensarkome, machen mit einer Inzidenz von ca. 0.5/100.000 pro Jahr lediglich 0.2% aller Malignome aus. Davon nimmt das Osteosarkom mit ca.35-40% Platz eins ein, gefolgt von Chondrosarkom (25%) und Ewingsarkom (16%) (AWMF Leitlinie, 2003). Das Osteosarkom tritt, obwohl es das häufigste Knochensarkom ist, somit lediglich 150- 200mal pro Jahr in Deutschland auf. 80% davon finden sich kniegelenksnah, also am distalen Femur oder an der distalen Tibia 10. Das typische Patientenalter liegt hier in der zweiten Lebensdekade.
Diese Erkenntnisse lassen sich jedoch nicht ohne Weiteres auf Fuß- und Sprunggelenk übertragen. Patientenalter, Dauer der Symptome bis zur korrekten Diagnose und Häufigkeitsverteilungen unterscheiden sich für die wichtigsten malignen Knochentumore an Fuß und Sprunggelenk zum Teil erheblich. Gleiches scheint für maligne Weichteilsarkome zuzutreffen. Weder das Liposarkom noch das pleomorphe Sarkom tauchen im Gegensatz zum restlichen Körper in den Statistiken der Fuß- und Sprunggelenkstumoren ganz oben auf. Lediglich das Synovialsarkom zeigt bei allen Untersuchern eine vergleichsweise hohe Prävalenz 578910.
Für die Praxis bedeutet dies, dass Fußtumoren besonders aufmerksam analysiert werden müssen. Statistiken zu Tumoren des gesamten Bewegungsapparats sind dabei meist wenig hilfreich oder können gar irreführend sein und die Diagnosefindung nur noch weiter erschweren.
Lokalisation
Im Krankengut von Ruggieri et al. 9 war ein Großteil der Knochentumore am Rückfuß (Talus und Calcaneus) lokalisiert (508/981, 51,8%), 24,6% (241/981) am Mittelfuß (übrige Fußwurzelknochen und Metatarsalia) und 23,6% (232/981) an den Phalangen der Zehen. Weichteiltumoren fanden sich zu 27,5% (52/189) am Rückfuß, zu 59,3% (112/189) am Mittelfuß und zu 13,2% (25/189) im Bereich der Zehen. Dieses Verteilungsmuster deckt sich weitestgehend mit den eigenen Beobachtungen, wobei die häufigsten, gutartigen Knochentumoren im eigenen Krankengut an Talus und Calcaneus, der distalen, sprunggelenksnahen Tibia und den Zehen zu finden waren. Bösartige Knochentumoren fanden sich ebenfalls überproportional häufig am Rückfuß. Weichteiltumoren, sowohl benigne als auch maligne, waren zu annähernd gleichen Teilen in allen o.g. Bereichen lokalisiert.
Ätiologie
Die Pathogenese gutartiger Knochenläsionen ist ungeklärt. Eine mögliche Ursache scheint in einem anachronistischen Verhalten bestimmter Zelltypen zu liegen. So wird für gewisse gutartige chondrogene Tumoren wie dem Enchondrom und Osteochondrom eine räumliche und zeitliche Fehlleitung von proliferierenden Chondrozyten aus der Wachstumsfuge angenommen, die zu einem Persistieren von Knorpelzellen an falscher Stelle führt. Andere Erklärungsversuche beinhalten traumatische oder hämodynamische (z.B. juvenile Knochenzyste) Ursachen. Bei der hereditären Exostosenkrankheit ist ein autosomal dominant vererbter Gendefekt bekannt (EXT-Gene). Andere Syndrome, wie der M. Ollier (Enchondromatose) und das Mafucci-Syndrom sind nicht vererblich, sondern weisen spontane Genmutationen auf.
Maligne Knochentumoren, Metastasen und hämato-onkologische Erkrankungen ausgenommen, können in seltenen Fällen auf dem Boden vorbestehender „precursors“ entstehen. Dabei stellen M. Paget, Bestrahlung, Knocheninfarkte, chronische Osteomyelitis und einige vorbestehende gutartige Knochentumoren die am besten bekannten präkanzerösen Veränderungen dar. Der Großteil primär maligner Knochentumoren entsteht jedoch „de novo“.
Die Ätiologie der meisten gut- und bösartigen Weichteiltumoren ist ebenfalls unbekannt. In seltenen Fällen wurden genetische Einflüsse, Umweltfaktoren, Bestrahlung, virale Infektionen und Immundefekte mit der Entwicklung bösartiger Weichteiltumoren in Verbindung gebracht. Des Weiteren existieren vereinzelte Berichte von Weichteilsarkomen, die in Narbengewebe, neben Frakturen und in der Nähe von chirurgischen Implantaten entstanden. Die große Mehrheit der Weichteilsarkome scheint jedoch ebenfalls „de novo“, also ohne erkennbare Ursache zu entstehen (Fletcher, 2013).
Symptomatik
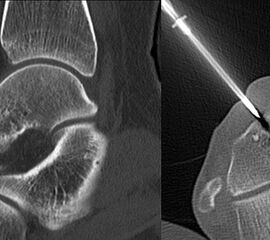
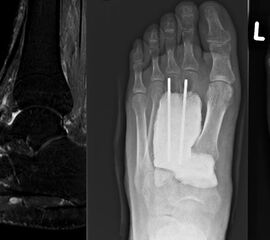
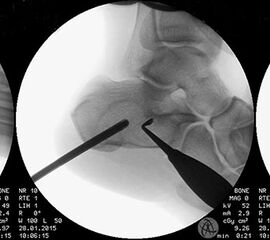
Die klinischen Symptome von Knochentumoren sind bis auf wenige Ausnahmen sehr unspezifisch. Schmerzen, Schwellung und Bewegungseinschränkungen können auch von zahllosen anderen krankhaften Prozessen ausgehen, insofern sind dementsprechende anamnestische Angaben nur zum Teil weiterführend. Knochenschmerzen zählen zu den somatischen Schmerzen und werden im Gegensatz zu neurogenen oder viszeralen Schmerzen meist als dumpf oder ziehend beschrieben. Neben der Qualität des Schmerzes kann aber auch die Intensität und das zeitliche Auftreten im Tagesverlauf hilfreiche Informationen liefern. Nachtschmerzen und ein positiver Aspirintest können beispielsweise konkrete Hinweise auf das Vorliegen eines Osteodiosteoms (Abb. 6) bieten. Der zeitliche Verlauf der beklagten Symptome kann Rückschlüsse auf das biologische Verhalten zulassen. So wachsen gutartige Tumoren in der Regel deutlich langsamer als aggressive, bösartige Neubildungen. Ausnahmen der Regel, so wie das Synovialsarkom, können jedoch falsche Sicherheit vortäuschen.
Eine pathologische Fraktur kann in einer zuvor asymptomatischen Person jedoch auch Erstmanifestation einer bislang unbekannten Knochenläsion darstellen, sowohl gut- als auch bösartiger Natur. Häufig erscheinen gutartige Knochentumore als Zufallsbefund, die es aber auch bei Beschwerdefreiheit weiter abzuklären gilt. Wird eine aggressive Knochenläsion oder ein schnell wachsender Weichteiltumor festgestellt, sollte immer nach einer möglichen B-Symptomatik gefragt werden.
Obwohl die Symptome maligner Knochentumore zunächst meist intermittierend und in Ruhe auftreten, nehmen die Schmerzen in der Regel an Intensität und Dauer kontinuierlich zu bis auch regelmäßige Nachtschmerzen bestehen und der Schmerz in benachbarte Gelenke ausstrahlt. Da die meisten Knochentumoren im Knocheninneren entstehen zeigt sich eine Schwellung meist erst dann, wenn die Kortikalis durchbrochen wird und der Tumor sich unter dem oder durch das Periost ausweitet. Aufgrund der sehr unspezifischen Anamnese und Symptome vergeht jedoch häufig eine lange Zeit bis ein aggressiver Tumor korrekt diagnostiziert wird. Eine Verzögerung in der spezifischen Diagnostik und Therapie dieser Läsionen kann folgenschwere Konsequenzen nach sich ziehen, da die Größe des Tumors einen prognostisch wichtigen Faktor für das rezidivfreie Überleben darstellt (Gollwitzer, 2012).
Körperliche Untersuchung
Bei der Inspektion des suspekten Befundes ist der Vergleich zur kontralateralen Körperseite heranzuziehen. Übliche Parameter wie Hautkolorit, Umfangsverhältnisse (Schwellung/Atrophie) und Stellung des Fußskeletts sind zu beachten. Bei der anschließenden Palpation sollte insbesondere auf die Verschieblichkeit des Tumors zu Haut und tieferen Gewebeschichten sowie zu den angrenzenden Sehnen geachtet werden. Eine Schmerzprovokation ist generell unspezifisch. Kann jedoch ein scharfer, elektrisierender Schmerz im Sinne eines positiven Tinel-Zeichens ausgelöst werden, so muss differenzialdiagnostisch an eine tumorbedingte Nervenirritation oder das Vorliegen eines neurogenen Tumors gedacht werden.
Eine besonders gründliche Untersuchung sollte immer bei pigmentierten Läsionen erfolgen, da sich das maligne Melanom überproportional häufig im Bereich des Fußes manifestiert 11. Im Zweifel sollte hier stets eine weiterführende Abklärung durch den Dermatologen und ggf. die Indikation zur histologischen Diagnosesicherung mittels Exzisionsbiopsie durch den Spezialisten erfolgen.
Diagnostisches Vorgehen
Die Ultraschalluntersuchung stellt in der Hand des erfahrenen Untersuchers ein geeignetes Mittel zur Differenzierung solider und flüssigkeitsgefüllter Weichteilformationen dar. Im Rahmen der tumororthopädischen Diagnostik ist jedoch eine spezifische Diagnosestellung durch die ausschließliche sonographische Untersuchung nicht möglich. Weitere diagnostische Schritte, meist in Form eines Röntgenbildes und einer Magnetresonanztomographie (MRT), müssen folgen 6. Zusätzlichen Stellenwert besitzt die Sonographie im Rahmen der bildgesteuerten Feinnadelpunktion 12.
Konventionelle Röntgenaufnahmen bleiben in der bildgebenden Diagnostik von Knochentumoren das wichtigste diagnostische Werkzeug. Zahlreiche Informationen können hierdurch einfach, kostengünstig und im Vergleich zu einigen alternativen Untersuchungsmethoden strahlungsarm eingeholt werden. Die in der konventionellen Diagnostik eruierbaren und zur weiteren Abklärung erforderlichen Informationen beinhalten Befunde zu Topographie der Läsion (Lokalisation im Fußskelett und im individuellen Knochenbereich), Begrenzungen der Knochenläsion, Art der Osteodestruktion und Periostreaktion, radiologische Erscheinung der Tumormatrix (Zusammensetzung des Tumorgewebes, z.B. dystrophe Verkalkungen) sowie Verhalten und Ausmaß der Weichteilbeteiligung. Dabei sollte der abzubildende Knochen immer einschließlich der benachbarten Strukturen und angrenzenden Gelenke dargestellt werden. Die Röntgenaufnahmen sind stets in mind. zwei Ebenen anzufertigen. In Abhängigkeit der Beschwerden sind belastete Aufnahmen im Stehen anzustreben um zusätzliche Aussagen zur Statik zu erlangen. Die Schrägaufnahme des Fußes stellt eine sinnvolle Ergänzung zu den Standardeinstellungen (dorsoplantar/a.p. und streng lateral) dar um die Knochen des Fußskeletts möglichst überlagerungsfrei darstellen zu können. Ziel- und Spezialaufnahmen können bei Bedarf zusätzlich durchgeführt werden.
Auch weichteilige Prozesse können in Abhängigkeit ihres biologischen Verhaltens Veränderungen im herkömmlichen Röntgenbild hervorrufen. Nicht selten finden sich bei langsam wachsenden Weichteiltumoren sklerotisch abgrenzbare Druckarrosionen des Knochens (z.B. PVNS). Auch Kalzifikationen und Ossifikationen des Tumorgewebes können hilfreiche Informationen zur potentiellen Tumorentität liefern.
Eine wichtige, weil unmittelbar therapie-relevante Einteilung tumor-assoziierter Knochenläsionen bietet die Klassifikation von Lodwick an. Die auf dem Röntgenbild sichtbaren Reaktionen sind hierbei ein Index für die Wachstumsgeschwindigkeit sowohl benigner als auch maligner Knochengeschwülste 13. Damit bietet die Lodwick-Klassifikation eine direkte Entscheidungshilfe zur Einleitung weiterer diagnostischer Maßnahmen (Schnittbildgebung, Biopsie) und der daraus folgenden Therapie, auch wenn definitive Aussagen zur Dignität nicht getroffen werden können.
| Ia | geographische Osteolyse, sehr langsam wachsend, immer sklerotischer und scharfer Rand |
| Ib | geographische Osteolyse, langsam wachsend, Knochenauftreibung >1 cm und/oder kein sklerotischer Rand |
| Ic | geographische Osteolyse, mittlere Wachstumsgeschwindigkeit, immer vollständige Kompaktapenetration |
| II | gemischt geographisches/mottenfraßartiges Wachstumsmuster, schnell wachsend |
| III | Ausschließlich mottenfraßartige und/oder permeative Destruktion, sehr schnell wachsend |
Nach Lodwick können die auf dem konventionellen Röntgenbild sichtbaren Destruktionsmuster in drei Hauptgruppen unterteilt werden: Rein geographische (umschriebene) Knochendestruktion, die eine langsame Wachstumsgeschwindigkeit widerspiegelt (Grad 1), gemischt geographisch/ mottenfraßartige Knochendestruktion mit permeativer Komponente, die eine intermediäre bis hohe Wachstumsgeschwindigkeit anzeigt (Grad 2) und rein mottenfraßartige oder permeative Destruktion, die Zeichen einer sehr schnellen Wachstumsgeschwindigkeit ist (Grad 3). Die erste Hauptgruppe unterteilt sich wiederum in sklerotisch deutlich abgrenzbare Läsionen (1a, sehr langsam wachsend), Osteolysen meist ohne Sklerosesaum und >1cm (1b, langsam wachsend) und weiterhin geographisch, also ausreichend gut abgrenzbare Osteolysen, welche obligat eine vollständige Kompaktapenetration aufweisen (1c, mittlere Wachstumsgeschwindigkeit) (Tab. 1, Abb. 7). Sobald eine Grad 1c Knochenläsion nach Lodwick vorliegt, müssen weitere diagnostische Schritte diskutiert werden. Diese beinhalten üblicherweise eine MR-tomographische Untersuchung, gefolgt von einer Biopsie.
Die Magnetresonanztomographie erlaubt nicht nur die exakte Beurteilung der intramedullären und extraossären Tumorausdehnung einschließlich reaktiver Zone, sondern auch die genaue Lagebeziehung zu neurovaskulären Strukturen (Abb. 8) und eine Differenzierung zwischen vitalen versus nekrotischen Tumoranteilen. Dies ist insbesondere für eine mögliche Biopsie von entscheidender Bedeutung um repräsentatives Tumorgewebe für die histopathologische Analyse gewinnen zu können. Die bei Verdacht auf einen Knochen- oder Weichteiltumor vom Radiologen durchzuführenden Standardprotokolle der MRT wurden im Jahr 2006 von der Arbeitsgemeinschaft Muskuloskelettale Diagnostik der Deutschen Röntgengesellschaft veröffentlicht (Tab.2) und gewähren bei entsprechender Umsetzung eine qualitativ hochwertige Untersuchung (DRG, 2006).
| Parameter: FOV angepasst, Schichtdicke angepasst Anmerkungen: Spulenwahl nach Lokalisation und Ausdehnung des Tumors (Röntgenbild obligat!). Bei Osteo- und Ewing-Sarkom zunächst koronar T1 SE über gesamten tumortragenden Knochen (Bodyspule, Body-Phased-Array-Spule) zum Ausschluss/Nachweis von "Skip"-Läsionen, dann möglichst auf höher auflösende Spule wechseln und nach oben aufgeführtem Protokoll untersuchen (Deutsche Röntgengesellschaft, 2006). |
| 1) koronar oder sagittal T1 SE |
| 2) axial T2 FSE FS (Knochentumor) axial T2 FSE (Weichteiltumor) |
| 3) sagittal oder koronar T1 SE n. Gd (gleiche Ebene wie nativ) |
| 4) axial T1 SE FS n. Gd |
Je nach vermuteter Tumorentität können zusätzliche Sequenzen durchgeführt werden (z. B. Häm-Sequenzen bei pigmentierter villonodulärer Synovialitis). Bestimmte Tumorentitäten können alleine durch die MRT-Untersuchung aufgrund ihres typischen Signalverhaltens diagnostiziert werden 146. Aufgrund der Seltenheit und der großen Heterogenität muskulo-skelettaler Tumoren sind spezielle Fragestellungen zu diesem Thema aber auch für eine Vielzahl von Radiologen nicht alltäglich. Es empfiehlt sich deshalb, im Zweifelsfall die Zweitmeinung eines tumororthopädischen Zentrums einzuholen (Link für Online-Konsil im Anhang).
Die Computertomographie (CT) wird seltener als die MRT herangezogen um eine spezifischen Artdiagnose zu finden, liefert aber wertvolle Informationen zur Kortikalisbeschaffenheit (Kontinuität, Stärke, enostale Arrosion) unterschiedlichster Knochenläsionen. Insbesondere die enostale Kortikalisarrosion, wie sie häufig bei chondrogenen Tumoren anzutreffen ist, kann konkrete Hinweise liefern, die in Zusammenschau mit histologischen Befunden zu einer definitiven Diagnose führen (siehe Spezifische Entitäten: Enchondrom vs. atypischer chondrogener Tumor/Chondrosarkom). Die Computertomographie ist außerdem hilfreich in der Abgrenzung komplexer anatomischer Strukturen (z.B. 3D-Rekonstruktion) und sehr kleiner Knochenläsionen. Bei der Diagnose des Osteoidosteoms bleibt die CT Mittel der Wahl um die charakteristischen Veränderungen in der bildgebenden Diagnostik exakt darzustellen (Abb. 6). Die Gewebedichte von weichteiligen Tumoren, insbesondere von intra- und extraossären Lipomen, kann im Vergleich zum subkutanen Fettgewebe mithilfe der Houndsfield-Skala beurteilt werden.
Im Rahmen des onkologischen Stagings maligner Erkrankungen des Bewegungsapparats bleibt die CT aufgrund ihrer hohen Auflösung ebenfalls Mittel der Wahl, eine Metastasierung und disseminiertes Tumorwachstums darzustellen.
Nuklearmedizinische Verfahren wie die Szintigraphie, Positronen-Emmissions-Tomographie oder Hybridsysteme (SPECT, PET-CT, PET-MRT) spielen in der primären Artdiagnostik muskulo-skelettaler Tumoren meist eine nur untergeordnete Rolle, sind aber für das Staging maligner Tumoren und die Metastasensuche disseminierter Tumorerkrankungen wichtige Werkzeuge der bildgebenden Diagnostik. PET-Verfahren können dabei den Knochen- und Glucosestoffwechsel hervorragend darstellen, in Kombination mit den klassischen Schnittbildverfahren können außerdem die Knochenmorphologie (PET-CT) und ein Knochenmarksbefall (PET-MRT) beurteilt werden 15.
Trotz der zunehmenden Genauigkeit bildgebender Untersuchungen kann auch ein in diesem Spezialgebiet erfahrener Radiologe häufig nur eine Differentialdiagnose anbieten. Sofern eine spezifische, eindeutig benigne Diagnose klinisch und radiologisch nicht gestellt werden kann, ist eine Biopsie anzustreben 16. Die definitive Diagnosesicherung erfolgt durch den Pathologen auf der Basis der Analyse von Biopsiematerial. Ort und Art der Biopsie werden durch die Lokalisation des Tumors vorgegeben. Vor der Biopsieentnahme ist der definitive operative Zugangsweg für die anschließende Tumorresektion festzulegen. Entscheidend für die Lokalisation der Probebiopsie ist nicht zwangsläufig eine möglichst kurze Wegstrecke zum Tumor, sondern vielmehr die Schonung tumorfreier Kompartimente und der für den Extremitätenerhalt relevanten Strukturen 1718. Knöcherne Läsionen sollten prinzipiell vom Fußrücken her biopsiert werden, wohingegen ein direkter Zugang für alle Weichteilläsionen angezeigt ist. Neben der Entnahme von Tumorproben für die histopathologische Aufarbeitung sind stets auch Proben für eine mikrobiologische Analyse zu gewinnen (DD Osteomyelitis / Abszess). Gerade am Fuß ist nach knöcherner Biopsie einer pathologischen Fraktur durch Entlastung vorzubeugen. Für die Biopsiegewinnung stehen dabei unterschiedliche Methoden wie die Feinnadelaspirationszytologie (FNA), die perkutane Stanzbiopsie („core needle biopsy“, z.B. CT-gesteuert) oder offene chirurgische Biopsieformen zur Verfügung, welche mit unterschiedlichen Vor und Nachteilen vergesellschaftet sind 19.
Bei der offenen chirurgischen Biopsie unterscheidet man die häufiger durchgeführte Inzisionsbiopsie von der Exzisionsbiopsie, bei welcher der Befund mit der Biopsie komplett entfernt wird. Bei Letzterer muss durch die Bildgebung vorher die Diagnose als gesichert gelten. Andernfalls sind eine Inzisionsbiopsie oder eine perkutane, bildgesteuerte Biopsie (z.B. sonographisch gesteuerte Feinnadelbiospie, CT-Stanze) erforderlich. Der Vorteil einer Inzisionsbiopsie liegt in der Gewinnung einer großen Gewebeprobe, sodass die Diagnosestellung mit größerer Sicherheit erfolgen kann, die Nachteile in einem höheren Aufwand und Kosten sowie der Notwendigkeit einer Narkose und den allgemeinen Risiken einer (offenen) Operation (Infektion, Hämatom, pathologische Fraktur). Zur Vermeidung von Komplikationen empfiehlt es sich, bereits die Biopsie an der Institution durchzuführen zu lassen, welche auch die definitive Versorgung übernehmen wird. Studien zeigen, dass sich die Rate an Komplikationen in Diagnose und Behandlung muskulo-skelettaler Tumoren verdoppelt, wenn die Biopsie nicht an einem spezialisierten Tumorzentrum durchgeführt wird 17.
Staging
Fußtumoren werden ebenso wie andere muskulo-skelettale Tumoren nach dem Staging System von Enneking /MSTS klassifiziert 20. Gutartige Knochentumoren werden als G0 bezeichnet, bösartige üblicherweise in G1 (gut differenziert, niedrig maligne, low-grade), G2 (mäßig differenziert, high-grade) und G3 (schlecht differenziert, hoch maligne, high-grade) unterteilt (Fletcher, 2013). Für gutartige Knochentumoren ist insbesondere darauf hinzuweisen, dass es sich nicht um eine starre Klassifikation handelt. So können bestimmte Entitäten wie z.B. das Enchondrom in Abhängigkeit klinischer und radiologischer Befunde (z.B. Schmerzen, Größenprogredienz, Lokalisation) sowohl als inaktive Form (Stage 1) als auch als aktive (Stage 2) oder aggressive Form (Stage 3) vorliegen (Abb. 9,). Andere Tumorarten wie das Osteoidosteom (Stage 1) oder der Riesenzelltumor (aggressiv, Stage 3) sind aufgrund ihrer weniger variablen Biologie immer nur einer Kategorie zugehörig (Tab. 3).
| Stage1 | Stage2 | Stage3 | |
|---|---|---|---|
| Graduierung | G0 | G0 | G0 |
| Lage | T0 | T0 | T1-2 |
| Metastasen | M0 | M0 | M0 |
| Klinischer Verlauf | Latent, inaktiv, statisch, selbstheilend | Aktiv, progredient, expandierend | Aggressiv, invasiv, Knochengrenzen überschreitend |
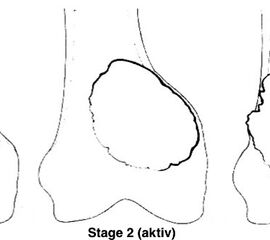
Dieses Stagingsystem beruht auf der Überlegung, dass anatomische Kompartimente (z.B. ein Knochen oder eine Muskelloge) natürliche Grenzen aufweisen, die einer Tumorausdehnung bis zu einem gewissen Grad entgegenwirken.
Am Fuß existieren neun funktionelle Faszienkompartimente (mediales, superfiziell-zentrales, laterales, Adduktor-, vier interossäre und das calcaneare/tief-zentrale Kompartiment), die insbesondere für die Einteilung und Therapie von Kompartmentsyndromen Relevanz besitzen (Sands, 2015).
Aus onkologischer Sicht ergibt sich jedoch eine andere Betrachtungsweise, da die dünnen Fasziengrenzen am Fuß im Gegensatz zu anderen Körperregionen von aggressiven Neubildungen leicht durchbrochen werden. Insofern können am Fuß drei prinzipielle Kompartimente identifiziert werden: Die knöchernen Kompartimente, welche durch Kortikalis und Periost begrenzt werden, das Kompartiment der Gelenke, welches durch Kapsel und Ligamente begrenzt ist und die muskulären Kompartimente, deren Grenzen durch die dünnen Muskelfaszien meist nur unzureichend definiert werden (Mercuri, 2002). Bestimmte Bereiche, wie das subkutane und perivasale Gewebe sind definitionsgemäß stets extrakompartimentell. Die Anatomie und somit auch die Kompartimente unterscheiden sich wesentlich zwischen Vor-, Mittel- und Rückfuß. Am Vorfuß einschließlich Metatarsalia stellen die einzelnen Strahlen (Metatarsalia und Phalangen) separate Kompartimente dar. Die proximal der Metatarsalia gelegenen Bereich werden z.T. auch als extrakompartimentell betrachtet, Kompartmentresektionen richten sich hier eher nach funktionell-anatomischen Überlegungen (z.B. Chopart-Amputation) als nach echten Kompartimenten.
Therapeutisches Vorgehen
Nicht jede tumoröse Neubildung muss zwangsläufig therapiert oder operiert werden. Läsionen, welche in der Kombination klinischer und radiologischer Befunde eindeutig einer spezifischen benignen Entität zugeordnet werden können (spezifische Diagnose), die mechanische Festigkeit des Knochens nicht gefährden und asymptomatisch sind, können grundsätzlich im Verlauf beobachtet werden. Dies trifft beispielsweise für das nicht ossifizierende Fibrom (NOF), das Osteochondrom oder das Enchondrom zu, kann aber auch für ein oberflächlich gelegenes Lipom oder ein mit Sicherheit diagnostiziertes Ganglion der Fall sein, das keine Beschwerden verursacht 16.
Die operative Therapie von Fußtumoren unterscheidet sich grundsätzlich nicht von anderen Lokalisationen und orientiert sich an den bekannten Prinzipien der Einteilung und Therapie gut- und bösartiger muskulo-skelettaler Neoplasien von Enneking 2120. Die unterschiedlichen Varianten der operativen Tumorresektion sind anhand ihrer Resektionsränder in intraläsionale, marginale, weite und radikale Resektionen einzuteilen. Die Planung der individuellen operativen Therapie, welche neben der Tumorresektion auch die anschließende Rekonstruktion beinhaltet, wird jedoch von zahlreichen weiteren Faktoren beeinflusst. Biologisches Alter, Lebenserwartung, Aktivitätsanspruch, Compliance und persönliche Präferenzen des Patienten müssen in eine gemeinsame Entscheidungsfindung einfließen. Kompromisse auf Kosten eines tumorradikalen Vorgehens dürfen bei kurativen Therapieansätzen niemals geschlossen werden. Eine interdisziplinäre Tumorkonferenz ist hier das zentrale Entscheidungsgremium. Relevante lokale Faktoren der chirurgischen Therapie sind die Ausdehnung des Tumors im Knochen, eine Gelenkbeteiligung sowie der Weichteilanteil mit Einbeziehung von neurovaskulären Strukturen und benachbarten Kompartimenten. Diesbezüglich kommt insbesondere der Magnetresonanztomographie (MRT) diagnostisch entscheidende Bedeutung zu.
Die Diagnose einer Infiltration der benachbarten Gefäß-Nerven-Scheide, welche generell eher selten ist, sollte nur bei eindeutigem Befund, d.h., wenn Tumorgewebe innerhalb oder um das neurovaskuläre Bündel erkennbar ist (>180° Ummauerung), gestellt werden 22.
Es bestehen jedoch einige fußspezifische Besonderheiten: Eine pneumatische Blutsperre, welche nach ausreichender Elevation und passiver Exsanguination des zu operierenden Beines aktiviert wird, ist einer Esmarch-Blutleere vorzuziehen, um das Tumorgewebe nicht zu traumatisieren und dadurch die Verbreitung von Metastasen zu begünstigen. Eine Ausnahme dieser Prozedur gilt für angiomatöse Tumoren wie der AV-Malformation oder dem cavernösen Hämangiom bei der bewusst eine Stauung durch eine Tourniquet genutzt wird, um die Raumforderung besser darstellen zu können. Die Tumorresektion erfolgt gemäß dem Grading der Läsion mit entsprechenden Resektionsgrenzen (intraläsional – marginal – weit – radikal). Aufgrund der begrenzten anatomischen Verhältnisse des Fußes sind ferner radikale Resektionen meist gleichbedeutend mit einer Strahlamputation und häufiger notwendig als am übrigen Bewegungsapparat. Sollte die unter onkologisch korrekten Gesichtspunkten durchzuführende Tumorentfernung die Resektion von plantaren Nerven beinhalten, muss eine (Teil-)Amputation des Fußes in Erwägung gezogen werden, da der Verlust relevanter senso-motorischer Strukturen hier einer funktionellen Amputation gleichkommt.
Adjuvantien bei intraläsionalen Eingriffen
Zahlreiche gutartige Knochentumoren können erfolgreich durch eine intraläsionale Curettage behandelt werden. Mithilfe der Diamantkopfhochfrequenzfräse kann ein makroskopisch tumorfreies Knochenbett geschaffen werden; der thermische Effekt des Fräsmechanismus wird durch das Unterlassen kontinuierlicher Kühlmaßnahmen (Spülung) zusätzlich erhöht. Ferner kann die Lokalrezidivrate einiger aktiver und aggressiver gutartiger Knochenläsionen durch den intraoperativen lokalen Einsatz chemischer oder thermischer Adjuvantien – wie Phenol, hochprozentigem Alkohol (Ethanol 95%), flüssigem Stickstoff oder Knochenzement aus Polyme- thylmethacrylat (PMMA) – zusätzlich gesenkt werden 2324. Das tumorzell-denaturierende Potenzial von PMMA ist im Vergleich zu etablierten Adjuvantien nicht ausreichend untersucht. Ein Vorteil der Plombage mit Knochenzement ist jedoch der unmittelbar stabilisierende Effekt auf die kürettierte Knochenhöhle sowie eine in bildgebenden Verlaufskontrollen zum umgebenden Knochengewebe gut sichtbare Abgrenzung (DD Rezidiv, Knochenheilung) 25.
Adjuvante und neoadjuvante, nicht-operative Therapieformen
Unter dem Begriff adjuvante und neoadjuvante, nicht-operative Therapieformen werden systemische und lokale, nicht-operative Therapiemaßnahmen zusammengefasst, die insbesondere in der Behandlung bestimmter Knochen- und Weichteilsarkome eine wichtige Rolle einnehmen und die Prognose maßgeblich beeinflussen können. Da der Einsatz von Chemo- wie auch Strahlentherapie jedoch maßgeblich von der jeweiligen Entität abhängt, sind pauschale Empfehlungen hierzu nicht möglich. Spezielle Therapieformen wie die isolierte Extremitätenperfusion (ILP/Isolated Limb Perfusion), bei welcher Zytostatika lokal in hohen Konzentrationen appliziert werden können, oder die lokale Hyperthermie, finden auch an Fuß- und Sprunggelenk Anwendung, bleiben jedoch Spezialzentren vorbehalten 26. Die Behandlung muskulo-skelettaler Tumoren erfordert meist eine multidisziplinäre Behandlungsstrategie. Die besten Ergebnisse werden nachweislich von erfahrenen Tumorchirurgen in spezialisierten Tumorzentren erzielt. Jeder Patient sollte deshalb in einer interdisziplinären Tumorkonferenz diskutiert werden, welche eine gemeinschaftliche und definitive Therapieempfehlung abgibt. Neoadjuvante und adjuvante Behandlungsmodalitäten wie Chemo- oder Strahlentherapie sind dabei wesentlich für die Verbesserung der Prognose und Überlebensraten sowie die lokale Kontrolle in der Behandlung primärer maligner Neoplasien, insbesondere dem Osteo- und Ewing-Sarkom, verantwortlich. Die neoadjuvante Bestrahlung oder Brachytherapie findet ihre Anwendung hauptsächlich in der Therapie schlecht differenzierter Malignome mit zu erwartenden knappen Resektionsrändern oder bei Lokalisation in enger Nachbarschaft zu neurovaskulären Strukturen. Prinzipiell werden bei der Bestrahlung des Fußes aufgrund des erhöhten Risikos einer radiogenen Fibrose oder Stressfraktur geringere Strahlendosen appliziert (Gollwitzer, 2013).
Prinzipien der operativen Therapie
Knochentumore
Intraläsionale Resektion /Curettage:
Bei gutartigen latenten oder aktiven tumorösen Knochenläsionen (Stage 1 und 2 nach Enneking) an Fußes und Sprunggelenk stellt die Curettage das Verfahren der Wahl da. Die operative Durchführung mit Entfernung der entsprechenden Läsionen durch den scharfen Löffel mit nachfolgender Abtragung der reaktiven Zone und sklerotischen Begrenzung, am besten mithilfe einer Diamantkopf-Hochfrequenzfräse, ist technisch meist einfach durchführbar. Ein Großteil benigner Knochentumoren im Bereich des Fußes weist jedoch eine sehr enge Lagbeziehung zum subchondralen Knochen auf, so dass ein derartiges Vorgehen den Einbruch der Knochenhöhle in das jeweilige Gelenk mit entsprechender Verletzung des Gelenkknorpels zur Folge haben kann. Um ein Lokalrezidiv zu vermeiden, darf allerdings die gründliche Entfernung des periläsionalen Gewebes nicht unterlassen werden. Um eine onkologisch adäquate Versorgung zu gewährleisten, kann in Einzelfällen die Arthrodese des benachbarten Gelenks notwendig werden (Burgkart, 2003). Die Applikation intraoperativer Adjuvantien ist auch bei einer Vielzahl biologisch weniger aggressiven Läsionen sinnvoll, um das Rezidivrisiko weiter zu senken. Die anschließende Auffüllung (Plombage) der gründlich gereinigten Knochenläsion kann je nach Präferenz des Operateurs, Aktivität der Läsion (Rezidivgefahr) und Alter des Patienten mit autologem oder allogenem Knochen erfolgen. Des Weiteren stehen unterschiedlichste Knochenersatzmaterialien für diese Zwecke zu Verfügung. Die jeweiligen Vor- und Nachteile der einzelnen Verfahren (Entnahmemorbidität autologer Knochentransplantationen, reduzierte Osteointegration alternativer Verfahren, Kosten, etc.) sind individuell abzuwägen und auch von der Aggressivität des Tumors abhängig. Aggressive und rezidivfreudige, gutartige Läsionen wie der Riesenzelltumor oder die aneurysmatische Knochenzyste sollten primär nicht mit autologem Knochen versorgt werden. Hier empfiehlt sich bei gut zugänglichen Läsionen die temporäre Plombage mit Knochenzement, bis ein Rezidiv ausgeschlossen werden kann. Der Knochenzement bietet nicht nur eine unübertroffen hohe Primärstabilität und zusätzliche adjuvante thermische Wirkung auf die Knochenhöhle, sondern erleichtert auch die bildgebenden Verlaufskontrollen und Abgrenzung eines möglichen Rezidivs enorm. Zu beachten ist, dass insbesondere bei jungen Patienten PMMA-Zement nur eine temporäre Lösung darstellen sollte, da der Knochen hierdurch langfristig ausgedünnt werden kann. Der thermische Effekt kann außerdem negative Auswirkung auf den meist in unmittelbarer Nachbarschaft liegenden Gelenkknorpel haben 27. Unterschiedliche Knochenarten und -ersatzmaterialien sollten wenn möglich nicht miteinander gemischt werden da dies bildgebende Verlaufskontrollen per MRT und eine Beurteilung von Integration, Reaktion und Rezidiv deutlich erschweren kann.
En-bloc Resektion
Die im Vergleich zu übrigen Körperregionen bei aggressiven gutartigen oder niedrig malignen bösartigen (low-grade, G1) Knochentumoren praktizierte en-bloc Resektion ist am Fuß aufgrund der limitierten anatomischen Verhältnisse meist einer weiten Resektion mit Kontinuitätsunterbrechung gleichzusetzen. Insofern spielt diese Art der Tumorresektion hier eine nur untergeordnete Rolle.
Weite Resektion
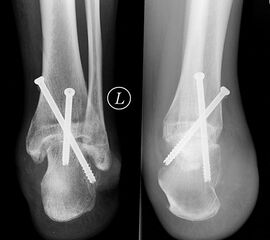
Bei der operativen Therapie maligner Neoplasien ist im Rahmen eines kurativen Therapieansatzes die weite Resektion zwingend erforderlich. Dabei richtet sich das jeweilige operative Vorgehen mit der nachfolgenden Rekonstruktion nach der Lokalisation des Tumors. Bei Läsionen im Bereich der distalen Tibia ist eine Segmentresektion des Knochens mit möglicher Überbrückung des Defekts durch Verwendung eines Tibia-Verschiebespans oder Fibula-Autografts und gleichzeitige Arthrodese im Bereich des oberen Sprunggelenks möglich. Aufgrund der hohen Belastung in diesem Extremitätenabschnitt ist eine Doppelung der Fibula und Anlagerung zusätzlicher Beckenkammspongiosa zu diskutieren (Burgkart, 2003). Bei Neoplasien im Bereich der distalen Fibula kann mit segmentaler Resektion des betroffenen Knochenabschnitts inklusive lateralem Malleolus und Durchführung einer tibio-talaren Arthrodese mit geringgradiger Extremitätenverkürzung meist ein funktionell gutes Ergebnis erzielt werden. Ist der Knochentumor im Bereich der posterioren Talusanteile lokalisiert so kann nach Osteotomie im Bereich des Talushalses unter Verkürzung der Extremität eine tibiocalcaneare Arthrodese mit Einbeziehung des restlichen Talus im Sinne einer Blair-Arthrodese durchgeführt werden 28. Bei Tumoren im Bereich des Calcaneus, die eine weitere Resektion notwendig machen, ist entweder eine Syme-Amputation oder die isolierte Resektion des Calcaneus mit Versorgung des entstandenen Defekts durch einen myo-cutanen Lappen und Verwendung spezieller Schuhe möglich (Burgkart, 2003). Ausgeprägte Befunden, die über die Höhe des oberen Sprunggelenks hinausreichen, erfordern selten eine distale Unterschenkelamputation (Abb. 10a-e). Die früheren Amputationsschemata, die von Amputationen in der distalen Hälfte des Unterschenkels abgeraten haben, besitzen heute keine Gültigkeit mehr 29. Dem Erhalt der Länge ist nach Beachtung einer entsprechenden Radikalität der Tumorresektion höchste Priorität zu bemessen. Bei Tumorlokalisation im Bereich des Mittelfußes können nach vollständiger Entfernung des jeweiligen Knochens Rekonstruktionen unter Verwendung autologer oder allogener struktureller Transplantate ("strut grafts") zu funktionell guten Mittelfußarthrodesen führen (Abb. 11) (Burgkart, 2003). Mit Ausnahme der großen Zehe können Amputationen der Zehen meist gut kompensiert werden. Amputationen in Höhe der Grund- und Mittelglieder der Kleinzehen sind wegen der Imbalance der Muskulatur mit sekundären Fehlstellungen zu vermeiden 29.
Entsprechende Amputationen des Fußes bleiben das Mittel der Wahl, falls eine adäquate lokale Tumorresektion aus onkologischen Gesichtspunkten nicht möglich ist. Kompromisse auf Kosten eines tumorradikalen Vorgehens dürfen bei kurativen Therapieansätzen niemals geschlossen werden 2510.
Weichteiltumoren
Marginale Resektion
Benigne Weichteiltumoren werden zumeist marginal reseziert, d.h. knapp außerhalb oder, falls vorhanden, mit der Pseudokapsel des Tumors, jedoch ohne einen Mantel gesunden Gewebes zusätzlich zu entfernen. Diese Form ist für primär maligne Tumoren nicht geeignet.
Weite Resektion
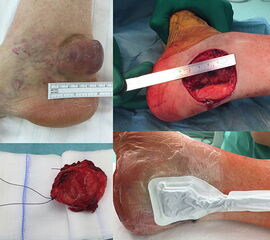
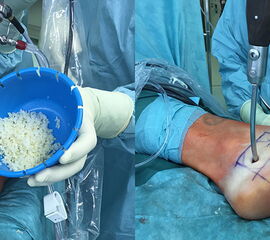
Hierbei wird der Tumor mit einem entsprechenden Sicherheitsabstand, also einem Mantel gesunden Gewebes entfernt. Eine genaue Definition des notwendigen Abstands in Zentimetern ist kaum möglich da unterschiedliche Gewebearten eine unterschiedliche Barriere für Tumorzellen darstellen. Weite Resektionen für mittel- oder schlechtdifferenzierte Malignome sind aufgrund des geringen Weichteilmantels über dem knöchernen Skelett im Bereich des Fußes und Sprunggelenks mit onkologisch ausreichendem Abstand und dennoch innerhalb des Kompartiments selten sinnvoll durchführbar. Bei größeren Tumorausdehnungen müssen häufig weite Anteile der Weichteildeckung reseziert werden was plastisch-chirurgische Deckungen nach sich zieht. Ist ein primärer Wundverschluß nicht möglich, so werden entsprechende Defektwunden zwischenzeitlich häufig per Vacuumversiegelung verschlossen bis die histopathologische Analyse abgeschlossen ist und einen mikroskopisch vollständigen Resektionsstatus im Gesunden (R0) bestätigt (Abb. 12 und 13).
Radikale Resektion
Die radikale Resektion umfasst die Entfernung des gesamten Kompartiments, von dem der Tumor ausgeht. Am Fuß ist dies häufig gleichbedeutend mit einer Amputation des betroffenen Extremitätenabschnitts.
Amputationen
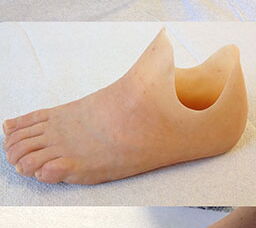
Bei Vorliegen einer malignen Tumorerkrankung sind Amputationen im Bereich des Fußes zur kurativen Behandlung häufiger notwendig als an anderen Körperpartien. Chou et al. berichten bei einem Anteil von 38,6% Malignomen bei 153 Tumoren des Fußes über eine Amputationsrate von 20,2%, entsprechend 52,5% aller Malignome 7. Dies ist einerseits der kompakten Anatomie des Fußes und dem Fehlen echter Kompartimente geschuldet, andererseits der Tatsache, dass ausreichend weite Sicherheitsabstände bei der Resektion maligner Tumorerkrankungen aus onkologischer Sicht am Fuß häufig nur durch Amputation möglich sind. Zahlreiche Amputationstechniken des Fußes ergeben zudem gute funktionelle Ergebnisse. Transmetatarsale Amputationen und Lisfranc-Amputationen erfordern nach Versorgung mit orthetischen Vorfußplatzhaltern oder einer Vorfußprothese nach Bellmann (Abb. 14) meist nur geringe Anpassungen am Konfektionsschuhwerk 30. Transmetatarsale Amputationen weisen häufig eine bessere Funktion und ein geringeres Risiko an Revisionsoperationen auf als Strahlamputationen, insbesondere als die kombinierte Resektion des 1. und 2. Strahls. Eine zwangsläufige Überbelastung der verbleibenden Mittelfußknochen führt in diesem Fall nicht selten zu Ulzerationen, welche weitere Amputationen erfordern (Chairmann, 1999). Im Gegensatz zur Teilamputation oder Amputation des zweiten bis vierten Os metatarsale, aus der lediglich eine geringfügige Verkleinerung der Standfläche resultiert, beeinträchtigen Amputationen am ersten und am fünften Strahl die Fußstatik nachhaltig 29.
Als Komplikation von Lisfranc- Amputationen werden regelmäßig postoperative Equinovarus-Fehlstellungen beobachtet. Dies lässt sich durch eine transossäre Reinsertion der Peronealsehnen und, falls nötig, Verlängerung der Achillessehne sowie konsequente postoperative Redression in einem Gips vermeiden. Ist ein plantigrades Auftreten gesichert, so können Patienten nach Amputationen in der Lisfranc-Linie teilweise auch ohne Prothese auskommen. Durch einen flachen Schuh mit harter Sohle und medialem Keilabsatz ist meist die Gehfähigkeit mit nur unwesentlichen Einschränkungen gegeben 29.
Chopart-Amputationen neigen aufgrund des vollständigen Fehlens der Ansätze der Dorsalextensoren und Pronatoren in noch größerem Maße zur Ausbildung einer Spitzfußstellung und Varuskontraktur (Abb. 15). Dies kann zu einer schlechteren Funktion als nach distalen Unterschenkelamputationen führen. Verhindert werden kann dies durch Reinsertion der Sehne des M. tibialis anterior und durch eine primäre Sicherung der Position durch einen tibiotalaren Fixateur externe oder sekundär durch eine Arthrodese des oberen und unteren Sprunggelenks. Als weiter proximal gelegene Amputationstechniken sind u. a. die Pirogoff-, Boyd- und Syme-Amputation beschrieben. Hierbei sind trotz osteoplastischer Modifikationen der einzelnen Techniken immer mehr oder weiniger große Beinlängendifferenzen zu erwarten 25. Bei der ursprünglichen Pirogoff-Amputation wird nach Talektomie das Tuber calcanei in die Malleolengabel geschwenkt und mit der Tibia fusioniert. Die Modifikation nach Boyd und Spitzy kann durch eine Vertikalisierung des lediglich im Bereich des Proc.anterior calcanei gekürzten Calcaneus eine geringere Beinverkürzung erzielen.
In Abbildung 16 wird der Fall eines 48-jährigen Patienten nach Boyd-Amputation aufgrund eines Chondrosarkoms des Mittelfußes demonstriert. Mit einem guten funktionellen Ergebnis konnte der Patient 6 Monate postoperativ sein Hobby Alpiner Skilauf wieder ausüben. Die Syme-Amputation beschreibt die Amputation im oberen Sprunggelenk, welche einen Unterschenkelstumpf hinterlässt. Sie wird dennoch zu den Rückfußamputationen gerechnet.
Vorausgesetzt eine vollständige Tumorresektion ist sicher und technisch sinnvoll möglich, bleibt auch bei tumor-assoziierten Amputationen im Sprunggelenks- und Unterschenkelbereich die Regel bestehen, so viel Länge wie möglich zu erhalten. Die ehemals gültigen Schemata [zur Verth’sches Amputationsschema (Baumgart, 2007)] haben durch Fortschritte der Orthopädietechnik und Rehabilitation nahezu keine Bedeutung mehr. Es ist heutzutage nicht mehr gerechtfertigt, auf Grund der Bedürfnisse der orthopädietechnischen Versorgung Amputationen höher anzusetzen als aus chirurgischer Sicht notwendig 31. Der Energieaufwand zwischen Amputationen im Fußbereich und auf Höhe des Unterschenkels unterscheidet sich beträchtlich (+50%), außerdem bringen propriozeptive Eigenschaften der Fußsohlenhaut dem Patienten wertvollste Rückkopplungen über die tatsächliche Belastung und die Fortbewegung, die keine noch so perfekte Prothese ersetzen kann. Wichtiges Kriterium für den Erhalt eines plantaren Aufsetzens bleibt außerdem, dass praktisch alle Stümpfe im Rückfußbereich endbelastbar sind. Die von Chou et al. attestierte Einschätzung, junge und aktive Patienten würden von einer Syme- oder Unterschenkelamputation möglicherweise funktionell mehr profitieren als von einer Chopart-Amputation (Chou, 2010), ist deshalb mehr als kritisch zu betrachten.
Entsprechend der Tumorlokalisation können individuelle Modifikationen notwendig werden. Als „innere Amputationen“ werden spezielle Resektionstechniken am Rückfuß bezeichnet, die meist in Kombination mit Arthrodesen eine Kontinuität zwischen Unterschenkel und Vorfuß ermöglichen (partielle oder totale Kalkanektomie, Talektomie oder kombinierten Resektion von Talus, Calcaneus und Malleolen; 32).
Spezifische Therapie
Im Folgenden werden ausgewählte Entitäten gut- und bösartiger Knochen - und Weichteiltumoren des Fußes detailliert dargestellt:
Benigne Knochentumoren
Gutartige Knochentumoren sind weitaus häufiger als ihre malignen Vertreter. Wie Daten spezialisierter tumororthopädischer Zentren ergeben, sind gutartige Knochentumoren mindestens 4-mal häufiger als bösartige Knochentumoren 789. Diese Zahlen repräsentieren jedoch nur die symptomatischen und mittels operativer Therapie behandelten Tumoren. Ein Großteil benigner Knochenläsionen bleibt aufgrund fehlender Symptomatik unentdeckt oder erscheint lediglich als Zufallsbefund, so dass das Verhältnis in Realität wohl noch deutlicher zu Gunsten gutartiger Läsionen ausfallen würde. Pathologische Frakturen können bei langsam wachsenden, asymptomatischen Knochenläsionen das erste Symptom der Erkrankung sein.
Enchondrom
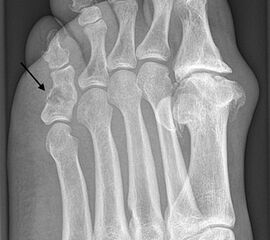
Das Enchondrom ist der häufigste Knochentumor im Bereich von Hand und Fuß und nach dem Osteochondrom der zweithäufigste gutartige Knochentumor überhaupt. Die geschlechtliche Verteilung ist ausgeglichen, Enchondrome finden sich meist bei Patienten zwischen 20-40 Jahren. Dieser chondrogene Tumor verhält sich meist asymptomatisch, kann aber durch eine Knochenexpansion und Schwellung sowie Spontanfrakturen (Abb. 17) auffallen. Radiologisch zeigen sich in der Regel gut abgrenzbare Osteolysen, Matrixverkalkungen sind typisch aber nicht obligat. Die MRT zeigt typischerweise eine annähernd flüssigkeitsäquivalente Signalqualität mit niedrigen Signalintensitäten in T1 und hoher Signalgebung in T2, die Binnenstruktur weist eine für chondrogene Tumoren typische Lobulierung mit KM-Aufnahme auf.
Im Gegensatz zu Osteochondromen ist die Lage von Enchondromen nicht auf die Metaphyse beschränkt. Sie finden sich auch im Bereich der Epi- und Diaphysen. Die kurzen tubulären Knochen der Metatarsalia und Phalangen sind bevorzugt betroffen. Hier findet sich die Läsion typischerweise im Bereich der proximalen Phalangen oder distalen Metatarsalia, eine Ausbreitung auf die gesamte Diaphyse ist von hier aus jedoch nicht ungewöhnlich. Die Möglichkeit einer malignen Entartung (Chondrosarkom) ist im Bereich der Metatarsalia und Phalangen im Vergleich zu den langen Röhrenknochen und platten Knochen extrem selten 33. Die übliche Therapie besteht in einer gründlichen Curettage. Je nach Größe des Defekts und Schwächung der Kortikalis kann die Transplantation eines stabilisierenden kortikospongiösen Spans notwendig werden. Zusätzliche osteosynthetische Verfahren sind nur selten erforderlich.
Das solitäre Enchondrom ist von Enchondromatosen, also disseminierten Enchondromen der Extremitäten und des Achsskeletts, abzugrenzen. Die Entartungswahrscheinlichkeit ist für Enchondromatosen wie dem M. Ollier (Abb. 18a und b) oder dem Maffuci-Syndrom deutlich erhöht und wird in der Literatur bis zu 25% angegeben. Klinische und radiologische Hinwiese für eine Entartung beinhalten Kortikalisveränderungen, wie -verdickung, -destruktion und die enossale Kortikalisarrosion, welche in der CT-Bildgebung mehr als 2/3 der Zirkumferenz des betroffenen (Röhren-) Knochens umfasst.
Das primäre, konventionelle Chondrosarkom des Fußes, welches nicht sekundär aus einem Enchondrom oder einer Exostose (exophytäres bzw. exostotisches Chondroarkom) sondern de novo entsteht, zeigt, ähnlich wie das Enchondrom, eine Prädilektion für die kurzen Röhrenknochen (Abb. 19). Das durchschnittliche Alter liegt hier bei 52 Jahren mit einer Bevorzugung des männlichen Geschlechts. In Abhängigkeit der Lokalisation und Graduierung des Tumors umfasst die geeignete operative Therapie die intraläsionale Curettage (G1) bis hin zur Amputation (G3) 34. Das Chondrosarkom ist nicht Strahlen- oder Chemotherapie-sensibel. Eine vollständige chirurgische Resektion bleibt deshalb die einzig sinnvolle Therapiemöglichkeit.
Osteochondrom
Das Osteochondrom (syn. kartilaginäre Exostose) ist charakterisiert durch einen von der Metaphyse ausgehenden Knochenauswuchs mit Knorpelkappe und existiert prinzipiell in einer gestielten (“pedunculated“) und einer breitbasigen ("sessile") Form. Beide Varianten können am Fuß auftreten, die gestielte Form ist häufiger vorzufinden (Abb. 20). Betroffen sind v.a. junge Patienten im ersten oder zweiten Dezennium, das geschlechtliche Verhältnis ist ausgeglichen. Im Röntgen zeigt sich neben dem typischen Blumenkohl-artigen Aspekt der gestielten Version eine ununterbrochene Kortikalis, die MRT zeigt ebenfalls einen in die Läsion hineinreichenden Markraum. Eine OP-Indikation besteht bei mechanischer Irritation, Funktionseinschränkung, neurovaskulärer Kompromittierung, und selten auch aus kosmetischen Gründen.
Die Therapie besteht aus einer Resektion inkl. Periost, die wenn möglich nach Abschluß des Wachstums (Rezidivwahrscheinlichkeit) durchgeführt werden sollte. Die Entartungsgefahr zum exostotischen Chondrosarkom ist im Bereich der distalen Extremitäten äußerst gering (Abb. 10a-e), ein Malignitätsverdacht besteht bei einer im MRT nachweisbaren Knorpelkappendicke >2cm und einer Größenzunahme nach Wachstumsabschluß.
Eine für den Fußchirurgen interessante, weil im Bereich des Sprunggelenks bevorzugt anzutreffende, jedoch sehr seltene Differentialdiagnose zum Osteochondrom bietet die sog. Dysplasia hemimeletica epiphysalis (Trevor´s disease). Dabei handelt es sich um eine Exostosenkrankheit der Epiphysen, gekennzeichnet durch lokale Proliferation von osteochondralem Gewebe, die bevorzugt die untere Extremität betrifft (Abb. 21a-c). Typisch ist die unilaterale Manifestation an einer Körperhälfte (Freyschmidt, 2010).
Liegen mehrere Exostosen simultan vor, so ist eine hereditäre Exostosenkrankheit hoch wahrscheinlich (Abb. 22). Eine genetisch bedingte Störung der Chondrozytenreifung führt per autosomal dominanten Erbgang (mit inkompletter Penetranz bei weiblichen Individuen) neben einer Deformation und asymmetrischer Wachstumsverzögerung v.a. der langen Röhrenknochen zur Ausbildung multipler Exostosen. Das männliche Geschlecht ist doppelt so häufig betroffen. Das Entartungsrisiko wird mit 5-25% angegeben, betroffen sind hiervon aber hauptsächlich stammnahe Lokalisationen und platte Knochen. Auch hier ist die Dicke der Knorpelkappe und eine Größenprogredienz der Läsion nach Wachstumsabschlusses Hinweis für eine maligne Transformation (Fletcher, 2013).
Juvenile Knochenzyste
Die juvenile Knochenzyste (Syn. Solitäre Knochenzyste) findet sich am Fuß fast ausschließlich am Calcaneus im Bereich des Ward´schen Dreieckes bzw. im ventralen triangulären Bereich zwischen den Haupttrabekelgruppen (Diard´s Area 6) 3536. Eine physiologische Rarefizierung der Trabekelstrukturen in diesem Bereich muss strikt von tumorösen Raumforderungen differenziert werden 3738. Die Hauptindikation einer operativen Therapie stellen Schmerzen und eine drohende pathologische Fraktur dar (Abb. 23). Calcaneuszysten, die in der Koronarebene 100% des Querschnitts erreichen oder 30% der Sagittalebene einnehmen, gelten als potentiell frakturgefährdet und sollten auch bei Symptomfreiheit prophylaktisch operiert werden 3940 (Abb. 24). Da simple Knochenzysten nicht selten als radiologischer Zufallsbefund auffallen, kann auch die Tumorangst des Patienten eine Indikation darstellen. Eine differenzierte Aufklärung des betroffenen Patienten (und seiner Eltern) ist hier umso mehr erforderlich.
Sobald eine osteolytische Knochenläsion des Calcaneus erscheint, ist eine weiterführende Abklärung mittels MRT indiziert. Das intraossäre Lipom des Calcaneus lässt sich im Röntgen nur dann von der simplen Knochenzyste unterscheiden, wenn zentrale, dystrophe Verkalkungen vorliegen (Abb. 25). Diese auch als Nidus oder Sequestrum bezeichneten Kalzifikationen sind typisch, jedoch nicht obligat für das intraossäre Lipom.
Prinzipiell existiert eine Vielzahl an möglichen Behandlungsmethoden der juvenilen Knochenzyste. Diese reichen von perkutanen Cortison- oder Knochenmarkaspirat-Injektionen bis hin zu offener Curettage und autologer Spongiosa-Transplantation. Die Angaben der Rezidivwahrscheinlichkeit sind in Abhängigkeit der angewandten Prozeduren sehr unterschiedlich und schwanken zwischen 20-50% 41. Das Rezidivrisiko kann nach Meinung zahlreicher Autoren durch folgende Maßnahmen reduziert werden 424344: Mechanische Zerstörung der inneren Zystenwand (z.B. durch Curette, scharfen Löffel), Applikation chemischer oder thermischer intraoperativer Adjuvantien (95% Ethanol, Phenol, Cryotherapie) und die Schaffung eines Abflusses (kanülierte Schraube, Eröffnung des benachbarten Markraums). Diverse Studien konnten zeigen, dass die minimalinvasive, endoskopische Therapie calcanearer Knochenzysten sehr gute Ergebnisse liefert 4540. Unsere eigene Technik verbindet die Vorteile perkutaner, endoskopischer Verfahren mit der Transplantation von allogenem, spongiösem Knochen (Abb. 26 und 27, Video 1).
Tipps und Tricks: Calcaneuszysten, die in der Koronarebene 100% des Querschnitts des Knochens erreichen oder 30% der Sagittalebene einnehmen, gelten als potentiell frakturgefährdet und sollten auch bei Symptomfreiheit prophylaktisch operiert werden.
Maligne Knochentumoren
Die beiden häufigsten primären malignen Knochentumoren überhaupt, das Osteosarkom und Chondrosarkom, finden sich neben dem Ewing-Sarkom auch im Bereich des Fußes am häufigsten. Diese Tumoren können sich klinisch wie auch bildgebend sehr variabel darstellen, was die hohe Anzahl von Fehldiagnosen und verzögerten Diagnosestellungen erklären kann 25. Osteosarkome treten im Bereich des Fußes im Vergleich zu den typischen Lokalisationen (kniegelenksnah) durchschnittlich ca. 10 Jahre später auf (Abb. 15). Der Calcaneus ist die bevorzugte Lokalisation für Osteosarkome des Fußskeletts und ein Großteil dieser Tumoren ist schlecht differenziert (G3) 46. Das Verteilungsmuster des Ewing-Sarkoms ist noch heterogener. In einer Nachuntersuchung von 1997 zeigten sich 6 von 16 Ewing-Sarkomen im Bereich der Metatarsalia, 4 in den Phalangen, 3 im Calcaneus und jeweils eines im Talus und eines im Os navikulare 47. Das durchschnittliche Patientenalter unterscheidet sich nicht von den herkömmlichen Lokalisationen. Auffällig ist jedoch die erhebliche Diagnoseverzögerung. So vergehen bei einem Ewing-Sarkom-Befall des Fußes durchschnittlich 14 Monate von Beginn der Symptome bis zur korrekten Diagnosestellung, bei Lokalisation im Rückfuß sind es gar 22 Monate (Abb. 28). Die Therapie des Ewing- und Osteosarkoms des Fußes unterscheidet sich grundsätzlich nicht von der etablierten Behandlungsstrategie dieser Tumoren und umfasst in der Regel die neo-adjuvante Chemotherapie, weite Tumorresektion und anschließende adjuvante Chemotherapie. Die Strahlentherapie besitzt in der Behandlung des Ewing-Sarkoms unverändert einen hohen Stellenwert. Ewingsarkome sind definitionsgemäß stets schlecht differenziert (G3 bzw. G4), also hoch maligne. Das operative Vorgehen ist dieser Tatsache anzupassen.
Das Chondrosarkom des Fußes zeigt, ähnlich wie das Enchondrom, eine Prädilektion für die kurzen Röhrenknochen. Das durchschnittliche Alter liegt hier bei 52 Jahren mit einer Bevorzugung des männlichen Geschlechts. In Abhängigkeit der Lokalisation und Graduierung des Tumors umfasst die geeignete operative Therapie die intraläsionale Curettage (G1) (Abb.19) bis hin zur Amputation (G3) (Abb.10) 34.
Metastasen finden sich in den distalen Abschnitten der Extremitäten deutlich seltener als in den proximalen (Abb.29 und 30). Am Fuß sind Metastasen somit vergleichsweise selten anzutreffen (<1%). Lungenkarzinome stellen hierbei den häufigsten Primärtumor dar 48 (Abb.31).
Benigne Weichteiltumoren
Stellvertretend für gutartige tumoröse Weichteilgeschwulste soll hier die pigmentierte villo-noduläre Synovialitis (PVNS) als wohl häufigste gutartige Weichteilneoplasie des Fußes erörtert werden. Die PVNS nimmt als einzige Entität in allen größeren Studien zu Fußtumoren einen der drei vorderen Plätze ein. Als Synonym der extra-artikulären Form der PVNS ist der Begriff des teno-synovialen Riesenzelltumors gebräuchlich. Die sehnenscheiden- und gelenkkapselreiche Fußanatomie prädestiniert für die Entstehung einer PVNS (Abb. 32). Das weibliche Geschlecht ist doppelt so häufig betroffen, das bevorzugte Alter liegt zwischen 30-50 Jahren. Eine schmerzlose, nur langsam größenprogrediente Schwellung ist das häufigste Symptom. Die Rezidivrate wird mit bis zu 30% angegeben 49. Bei der PVNS handelt sich um einen fibro-histiozytären Tumor (echte Neoplasie) und nicht wie ehemals angenommen um ein inflammatorisches oder posttraumatische Geschehen. Für die intraartikuläre Form, die wiederum in eine noduläre/lokalisierte und diffuse Form unterteilt werden kann, stellt das Sprunggelenk die dritt-häufigste Lokalisation am gesamten Körper dar (Abb. 33).
Im Röntgen zeigt sich gelegentlich eine gut abgrenzbare Weichteilformation (bei nodulärer Form) und knöcherne Druckarrosionen der angrenzenden Knochen. Sekundäre arthrotische Veränderungen der angrenzenden Gelenke sind möglich. Die MRT kann mit einem stark T2-gewichtetem Gradientenecho sog. Suszeptibilitätsartefakte der Hemosiderinablagerungen darstellen. Diese führen gewöhnlich zu charakteristischen Signalauslöschungen in T1 und T2 gewichteten Sequenzen. Eine Kontrastmittel-Aufnahme erfolgt in der Regel diffus und inhomogen. Die Therapie besteht in einer offenen Resektion. Wir raten dringend davon ab, intraartikuläre, lokalisierte Formen der PVNS per Arthroskopie resezieren zu wollen. Dieser Tumor sollte, wenn möglich, marginal und nicht intraläsional reseziert werden. Eine arthroskopische Zerkleinerung mit dem Shaver würde aus einer nodulären Form eine diffuse Form produzieren und die Rezidivwahrscheinlichkeit deutlich steigern. Ebenso ist vor einer Radiosynoviorthese (RSO) bei Vorliegen einer nodulären Variante abzuraten. Bei diesem nuklearmedizinischen Verfahren, welches gewöhnlich Anwendung bei chronisch entzündlichen Gelenkerkrankungen findet, werden Beta-Strahler in Gelenke injiziert. Ein therapeutischer Effekt hat sich bisher nicht nachweisen lassen.
Maligne Weichteiltumoren
Synovialsarkom
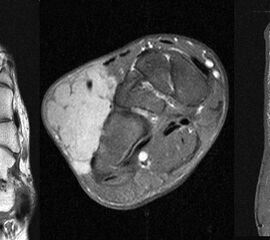
10% aller Patienten mit Weichteilsarkomen weisen bei Erstdiagnose bereits Metastasen auf, meist in der Lunge. Drei Viertel der Weichteilsarkome zeigen eine schlechte histologische Differenzierung („high-grade“, G3 und G4) und die Letalität beträgt insgesamt über 30%. Trotz des vergleichsweise seltenen Vorkommens (<1% aller Malignome) gilt diesen Entitäten aufgrund der schlechten Prognose erhöhte Aufmerksamkeit. Das Synovialsarkom ist der häufigste maligne Weichteiltumor im Bereich des Fußes und betrifft hier typischerweise Adoleszente und Erwachsene in der 2. bis zur 5.Lebensdekade (Abb. 34). Zwischen Beginn der Symptome und endgültiger Diagnosestellung vergehen durchschnittlich 21 Monate. Das Synyovialsarkom zeigt einen unspezifischen klinischen Verlauf mit variabler Wachstumsge- schwindigkeit und kann zahlreiche andere Entitäten imitieren 50. Die Gefahr sowohl pulmonaler/hämatogener als auch lymphogener Metastasen ist hoch.
Klarzellsarkom und Malignes Melanom
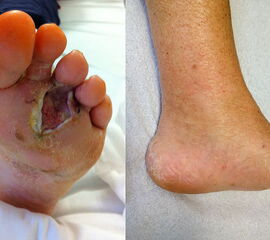
Das Klarzellsarkom ist ein äußerst seltener maligner Weichteiltumor (1% aller Weichteilsarkome), zeigt aber eine besondere Prädilektion für den Fuß und eine erhebliche Aggressivität. Bis zu 50% aller Klarzellsarkome finden sich hier 5152. Typisch ist eine tiefe, aponeurosen- und sehnennahe Lokalisation. Der Begriff „malignes Melanom der Weichteile“ wird aufgrund der histologischen Ähnlichkeit häufig synonym verwendet. Tatsächlich handelt es sich jedoch um separate klinisch-pathologisch Entitäten, deren Unterscheidung dem Pathologen nur molekularbiologisch, nicht aber immunhistochemisch möglich ist 51. Die Tumorgröße bei Erstdiagnose ist für das Klarzellsarkom wie auch für andere Weichteilsarkome der wesentliche prädiktive Wert der Prognose. Adjuvante Therapien sind wenig erfolgversprechend und so bleibt die weite Resektion die Therapie der Wahl 53.
Das klassische, kutane Melanom zeigt ebenfalls eine Prädilektion für den Fuß. Bei Frauen finden sich 42% aller malignen Melanome im Bereich der unteren Extremität. Ein Subtyp des kutanen Melanoms, das akrolentiginöse Melanom, weist eine besondere Vorliebe für den palmo-plantaren und subungualen Bereich sowie ein facettenreiches klinisches Bild auf 54 (Abb. 35). Dies unterstreicht die Notwendigkeit der genauen Inspektion im Rahmen der körperlichen Untersuchung. Eine zusätzliche dermatologische Abklärung sollte großzügig indiziert werden. Besondere Beachtung gilt bei beiden Entitäten dem sog. Sentinel-Lymphknoten, welcher bei Lokalisation eines Klarzellsarkoms oder malignen Melanoms der unteren Extremität in den Lymphabflusswegen der ipsilateralen Leiste entnommen wird und erhebliche prognostische Bedeutung besitzt 55.
Zusammenfassung
Fußtumoren treten, gemessen an der anteiligen Körpermasse des Fußes, überproportional häufig auf. Verteilungsmuster und -statistiken unterschiedlicher Studien belegen eine große Heterogenität. Zahlreiche seltene Tumoren und tumor-ähnliche Erkrankungen zeigen außerdem eine Prädilektion für den Fuß. Im Gegensatz zu den häufigsten Tumorlokalisationen muskulo-skelettaler Neoplasien (distales Femur, proximale Tibia, proximaler Humerus, subfaszialer Oberschenkel) können klassische Verteilungsmuster am Fuß nur selten Hilfestellung in der Diagnose bieten. Obwohl die kompakte Anatomie eine frühzeitige Erkennung von Neubildungen im Bereich des Fußes erleichtern sollte, wird das Ziel einer frühzeitigen Diagnosestellung häufig durch fehlendes Bewusstsein für Tumorerkrankungen der Fuß-und Sprunggelenksregion seitens des Arztes und des Patienten verfehlt. Die Erkennung suspekter Neubildungen erfordert selbst vom erfahrenen Orthopäden und Fußchirurgen in zahlreichen Fällen eine besondere Sensibilisierung für dieses spezielle Thema, um das sog. „diagnostische Fenster“ möglichst kurz zu halten.
Die definitive Diagnosestellung beruht auf der histopathologischen Analyse des Biopsiematerials oder Resektats. Die konventionelle Röntgenaufnahme ist erstes und wichtigstes Werkzeug in der bildgebenden Stufendiagnostik knöcherner Läsionen. Die Magnetresonanztomographie liefert in der weiterführenden Abklärung essentielle Informationen zu Tumorbeschaffenheit und -umgebung. Latente und einzelne aktive, gutartige Tumoren können in Zusammenschau der anamnestischen Angaben (z. B. Nachtschmerz), klinischen Befunden und einer radiologischen Stufendiagnostik durch eine Exzisionsbiopsie oder intraläsionale Curettage erfolgreich behandelt werden. Andere, in der differenzialdiagnostischen Abklärung als suspekt eingestufte Neubildungen werden üblicherweise einer offenen Probebiopsie oder bildgesteuerten Stanzbiopsie zugeführt. Die definitive Therapie maligner Neoplasien ist maßgeblich von einem vollständigen Staging der Tumorerkrankung abhängig. Für die lokale Beurteilung kommt insbesondere der MRT entscheidende Bedeutung zu (u. a. Tumorausdehnung, Infiltration von neurovaskulären Strukturen). Fernmetastasen müssen durch ein CT-Staging mit Untersuchung von Thorax, Abdomen und Becken ausgeschlossen werden. In besonderen Fällen können nuklearmedizinische Untersuchungen (PET-CT, Szintigraphie) notwendig sein. Bei der operativen Therapie maligner Neoplasien ist im Rahmen eines kurativen Therapieansatzes die weite Resektion zwingend zu fordern. Niemals dürfen Kompromisse zu Lasten der Tumorradikalität eingegangen werden. Entsprechende Amputationen des Fußes bleiben das Mittel der Wahl, falls eine adäquate lokale Tumorresektion aus onkologischen Gesichtspunkten nicht möglich ist. Adjuvante Therapieformen wie Strahlen- und Chemotherapie tragen wesentlich zur Verbesserung der Gesamtprognose in der Behandlung von bestimmten Malignomen bei. Bereits bei der Biopsie können Fehler eine primär vollständige Tumorresektion deutlich erschweren oder gar unmöglich machen. Inadäquat voroperierte Tumoren zeigen eine deutlich schlechtere Prognose. Aufgrund der Seltenheit dieses heterogenen und breiten Krankheitsbildes sollte im Interesse des Patienten im Zweifelsfall für Diagnose und Therapie die entsprechende Expertise eines muskulo-skelettalen Tumorzentrums mit spezialisierten Radiologen und Tumororthopäden/Fußchirurgen herangezogen werden 2510.
Anhang
Link zum Online-Konsil "muskuloskelettale Radiologie" des radiologischen Referenzzentrums für muskuloskelettale Erkrankungen der Technischen Universität München, Prof. Dr. med. Klaus Wörtler, Institut für diagnostische und interventionelle Radiologie, Klinikum rechts der Isar: https://konsil-msk.mri.tum.de/anmeldung/
Weitere Literatur
- AWMF online: Leitlinien der Deutschen Gesellschaft für Orthopädie und Orthopädische Chirurgie (DGOOC), Leitlinie Osteosarkom, 2003
- Baumgartner R, Bellmann D; Amputation und Prothesenversorgung, 2007, 3.Auflage, Thieme Verlag
- Burgkart R, Gradinger R, Tumoren des Fußes, in Fußchirurgie von Andreas B. Imhoff und Hans Zollinger-Kies, Thieme, 2003,pp. 291-305
- Campanacci, M., Bone and Soft Tissue Tumors: Clinical Features, Imaging, Pathology and Treatment. 2nd ed. 1999, Wien: Springer. 1319
- Chairman EL (1999) Principles and practice of podiatric medicine, 2. Aufl. Churchill, Livingstone, S 476– 477
- Chou LB (2010) Foot and ankle amputations: Lisfranc/Chopart. In: Wiesel SL (Hrsg) Operative techniques in orthopaedic surgery. Lippincott Williams & Wilkins, Philadelphia
- Dahlin DC, Unni KK: Bone Tumors: General Aspects and Data on 8,542 Cases. ed 4. Charles C Thomas, Springfield, IL: 1986.
- Deutsche Röntgengesellschaft (DRG) AG Muskuloskelettale Diagnostik; Fortschr Röntgenstr 2006; 178(1): 128-130: Von der AG Muskuloskelettale Diagnostik der Deutschen Röntgengesellschaft empfohlene Protokolle für MRT- Untersuchungen der Gelenke und Wirbelsäule
- Erlemann R, Wörtler K : Knochentumoren, Handbuch diagnostische Radiologie: Muskuloskelettales System 2,17. März 2005 von Jürgen Freyschmidt, A. Stäbler
- Fletcher C, Bridge JA., Hogendoorn PCW, Mertens F, WHO Classification of Tumours of Soft Tissue and Bone, World Health Organization Classification of Tumours, Lyon: 2013, Chapter 25: 348-362
- Freyschmidt J, Ostertag H, Jundt G: Knochentumoren mit Kiefertumoren: Klinik - Radiologie - Pathologie, April 2010, Springer
- Gollwitzer H, Toepfer A, Special Procedures in Foot and Ankle Surgery, Edition: 2013, Chapter: Tumors and Tumor-like Lesions of the Foot and Ankle: Diagnosis and Treatment, Publisher: Springer, Editors: Amol Saxena, pp.489-508
- Knöller S: Melorheostose, in Knochenkrankheiten von S.Peters, 2002, Steinkopff-Verlag Darmstadt
- Mercuri M, Casadei R, Foot and Ankle Surgery 2002 8: 175–190: Tumours in the foot
- Rüedi T, Murphy W., AO Principles of Fracture Management, 2000, S.58
- Sands A, Rammelt S, Manoli A 2nd, Fuß & Sprunggelenk 13 (2015) 11—21: Kompartment-Syndrom des Fußes — Eine klinische Übersicht
- Wirth CJ, Zichner L, Winkelmann W : Orthopädie und orthopädische Chirurgie: Tumoren und tumorähnliche Erkrankungen, 2004