Vorbemerkungen
Die systematische arthroskopische Inspektion des oberen Sprunggelenks (OSG) wurde erstmals 1939 von Tagaki (Tagaki 1939) beschrieben. Mangels geeigneter Instrumente konnte sich diese Technik zunächst nicht durchsetzen. Erst in den 70er Jahren fand die OSG-Arthroskopie zunehmend Anwendung. 1972 berichtete Watanabe über 28 OSG-Arthroskopien mit einer Fiberoptik (Watanabe 1972) und 1976 publizierte Chen seine Erfahrungen aus 67 Arthroskopien an Patienten und 17 Arthroskopien am Kadaver (Chen 1976). Seither ist die klinische Expertise in der Sprunggelenksarthroskopie signifikant gestiegen, so dass mittlerweile mehr als 10 Prozent aller arthroskopisch durchgeführten Operationen Gelenkspiegelungen am oberen Sprunggelenk sind (Hempfling 2001). Die OSG-Arthroskopie ist damit der dritthäufigste arthroskopische Eingriff nach den Knie- und Schultergelenkarthroskopien. Die straffe knöcherne und Führung des Talus in der Malleolengabel, die hohe Gelenkkongruenz sowie der in der Sagittalebene konvex-konkav geformte Gelenkspalt erschweren den arthroskopischen Zugang zum Gelenkraum. Anfänglich wurde die Arthroskopie überwiegend als diagnostisches Verfahren am OSG eingesetzt. Inzwischen haben sich die arthroskopischen therapeutischen und rekonstruktiven OP-Techniken zum Standardrepertoire der Fuß-und Sprunggelenkchirurgie etabliert.
Vorteile
- Aufgrund der minimal-invasiven Zugangswege besteht eine geringe Weichteiltraumatisierung mit einer verringerten postoperativen Morbidität.
- Die intraartikulären Knorpelflächen und pathologische Veränderungen im medialen, lateralen sowie zentralen Kompartiment können sehr gut visualisiert werden. Je nach Wahl des Zugangsweges kann die Darstellbarkeit bei der offenen Vorgehensweise limitiert sein oder sogar eine Malleolarosteotomie erforderlich sein.
- Geringe Komplikationsrate im Vergleich zu den offenen Operationstechniken am OSG.
Nachteile
- Limitierung der Zugangsmöglichkeiten bei engen Gelenkverhältnissen.
- Die Inspektion und Behandlung des dorsalen OSG-Gelenkkompartiments über die rein ventrale Arthroskopie ist oftmals erschwert und erfordert zusätzliche posteriore Portale und ggf. eine intraoperative Umlagerung des Patienten in Bauchlage.
Indikationen
- Synovialitis.
- Weichteilimpingement.
- Intraartikuläre Briden/Arthrofibrose.
- Knöchernes Impingement/Osteophyten.
- Freie Gelenkkörper/Chondromatosen.
- Traumatische chondrale und osteochondrale Flake Frakturen.
- Osteochondrale Läsionen.
- Subchondrale zystische Läsionen.
- Degenerative Gelenkveränderungen.
- Arthroskopische Arthrodese.
- Arthroskopisch gestützte Frakturversorgung.
- Arthroskopische Bandstabilisierung.
Anmerkung:
Hinsichtlich der Refixation frischer osteochondraler Fragmente liegen keine evidenzbasierten Richtlinen vor, bis zu welchem Ausmaß eine Refixation erfolgen sollte. Empfohlen wird eine Refixation ab einer Fragmentgröße von 15mm Durchmesser, wenn auf der Unterfläche ausreichend spongiöser Knochen vorhanden ist (van Dijk 2014). Die eingebrachten Implantate sollten unterhalb des Knorpelniveaus liegen 1.
Das arthroskopische Gelenkdebridement bei der OSG-Arthrose muss sehr differenziert eingesetzt werden. Es konnte nachgewiesen werden, dass Patienten mit einer lokalisierten Arthrose und einem Gelenkspalt von >2mm von einer Synovialektomie und Osteophytenabtragung mit Resektion chondraler Lappen profitieren, wohingegen bei generalisierten arthrotischen Veränderungen keine nachhaltige Verbesserung der Schmerzen und des Bewegungsumfangs zu erzielen ist 2,(Lampert 2011).
Limitierend bei der arthroskopischen Technik der OSG-Arthrodese sind Achsabweichungen. Lässt sich die Achse nicht auf physiologische Werte korrigieren, sollte auf ein offenes Verfahren gewechselt werden 34.
Kontraindikationen
- Lokaler Weichteilinfekt.
- Florider Gelenkinfekt.
Patientenaufklärung
- Teilbelastung mit 20kg an Unterarmgehstützen je nach operativem Verfahren für 5 Tage bis zu 6-8 Wochen postoperativ.
- Bei rekonstruktiven Verfahren wie z.B. Bandstabilisierungen und Frakturversorgungen oder nach einer arthroskopischen Arthrodese ist eine Versorgung mit einem Unterschenkelwalker für 6-8 Wochen erforderlich.
- Wundheilungsstörungen, Sensibilitätsstörungen (N. peroneus superficialis, N. peroneus profundus), Gefäßverletzungen (A. und V. tibialis anterior sowie deren Äste), Sehnenverletzung (Tibialis anterior-Sehne, Extensor digitorum longus-Sehne, Extensor hallucis longus-Sehne).
- Allgemeine Operationsrisiken.
Operationsvorbereitungen
- Röntgenaufnahme des OSG in 2 Ebenen (seitlich und Mortise view).
- Besteht der Verdacht eines knöchernen Impingementsyndroms sollte zur Darstellung der distalen Tibiavorderkante eine AMI-View (anteromedial impingement view) angefertigt werden, in der vor allem medial gelegene Osteophyten vollständig abgebildet werden 5. Hierbei handelt es sich um eine laterale Aufnahme des oberen Sprunggelenks, bei welcher der Strahlengang 45° kraniokaudal gekippt wird, bei Außenrotation des Beins von 30°.
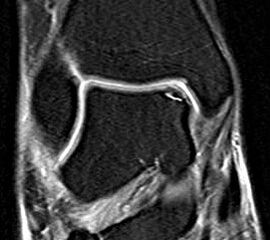
- MRT des OSG zur Beurteilung von pathologischen Weichteilveränderungen und Knorpelläsionen. Begleitende subchondrale Knochenödeme sind dabei ein Indikator für die Aktivität der Läsion.
- Ggf. CT zur Bestimmung der Lage und Größe von Osteophyten oder freier Gelenkkörper. Bei ausgedehnten osteochondralen Läsionen hilft das CT darüber hinaus, die Größe des Knochenschadens abzuschätzen.
- Dokumentation des Bewegungsausmaßes sowie der Durchblutung und der Sensibilität.
Instrumentarium
- 2,7 mm Arthroskop mit 30° Blickwinkel (optional 4 mm Optik mit 30° Blickwinkel).
- Shaversystem mit Weichteilresektoren sowie Kugel-, Zapfen- oder Walzenfräse (2,5-4,0mm Durchmesser).
- Rollenpumpe, Sauger, elektrolytfreies Arthroskopiemedium (z.B. NaCl-Lösung 0,9%).
- Bipolare Radiofrequenzsonde.
- Gebogenes Elevatorium, Küretten, Tasthaken. Spezielle Instrumente für die Arthroskopie kleiner Gelenke anstelle der Kniegelenkinstrumente sind hilfreich.
- Chondropicker/Ahlen zur Mikrofrakturierung.
- Alternativ: K-Drähte und Bohrmaschine zur Anbohrung.
- Ggf. Bildverstärker, sofern eine Frakturversorgung oder eine Arthrodese geplant ist oder die Entfernung von Osteopyhten und freier Gelenkkörper intraoperativ dokumentiert werden soll.
- Ggf. Osteosynthesematerial und resorbierbare Pins.
Anästhesie und Lagerung
- Intubationsnarkose, Larynxmaskennarkose, Spinalanästhesie.
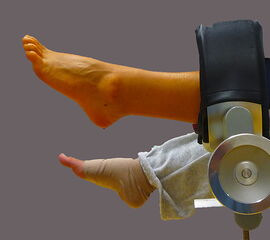
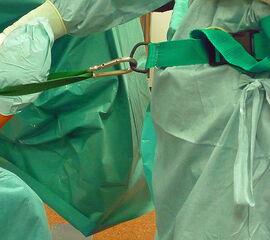
Fakultativ: Oberschenkel- oder Unterschenkelblutsperre (zwischen 350 und 250 mmHg, ca. 100 mmHg über dem systolischen Blutdruck). - Rückenlage. Bei außenrotiertem Bein Unterpolsterung der gleichseitigen Gesäßhälfte, so dass das OSG in einer Neutralstellung zu Liegen kommt. Die Füße überragen den OP-Tisch um etwa 30 cm, so dass das OSG auch von dorsal zugänglich ist, um ggf. posteriore Portale anlegen zu können. (Abbildung 1). Alternativ ist eine hängende Lagerung des Unterschenkels möglich.
- Mechanischer Beinhalter oder Beinschale.
- Bedarfsweise mechanischer Distraktor oder Fußschlaufe mit Gurt.
- Ggf. Strahlenschutzmatte für den Patienten.
Operationstechnik
Video 1
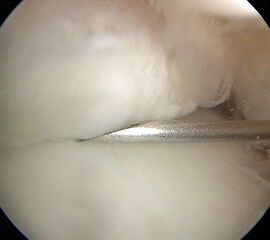
Einzeichnen der Landmarken und der medialen Begrenzung der Tibialis anterior-Sehne. Palpation des soft spots medial der Tibialis anterior-Sehne auf Höhe Gelenkspalts. Anlage des anteromedialen Portals durch vorsichtige Inzision der Haut mit dem Skalpell. Mit einem Klemmchen werden die Weichteile stumpf aufgespreizt und die Gelenkkapsel perforiert. Einführen der Trokarhülse mit einem stumpfen Obturator, Einführen des 2,7 mm Arthroskops.
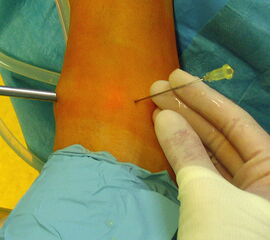
Abbildung 2 und 3
Mit Hilfe einer Kanüle unter arthroskopischer Sicht Identifikation der korrekten Lage des anterolateralen Portals lateral der Sehne des M. extensor hallucis longus. Die Kanüle sollte möglichst parallel zur Tibiavorderkante verlaufen, um intraoperativ eine gute Arbeitsrichtung der Instrumente zu gewährleisten. Inzision und Vorgehen analog zum anteromedialen Zugang.
Abbildung 4
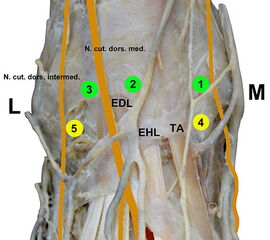
Übersicht der ventralen OSG-Arthroskopieportale:
1 = anteromediales Standardportal medial der Sehne der M. tibialis anterior (TA) auf Höhe des Gelenkspalts.
2 = zentrales Portal zwischen der Extensor digitorum longus (EDL)- und der Extensor hallucis longus-Sehne (EHL).
3 = anterolaterales Standardportal lateral der Sehne des M. extensor hallucis longus (EHL) auf Höhe des Gelenkspalts.
4 = akzessorisches tiefes anteromediales Portal ca. 1cm distal des anteromedialen Standardportals.
5 = akzessorisches tiefes anterolaterales Portal ca. 1cm distal und lateral des anterolateralen Standardportals.
L = lateraler Malleolus, M = medialer Malleolus; A. dorsalis pedis, N. cutaneus dorsalis medialis, N. cutaneus dorsalis intermedius.
Anmerkung:
Die Verwendung des anteromedialen und anterolateralen Standardportals ermöglicht eine gute Sicht auf den ventralen Gelenkanteil bis zum Talusdom. Intraoperativ ist in der Regel ein Portalwechsel erforderlich, um eine vollständige Inspektion der medialen und lateralen Gelenkanteile durchzuführen. Einige Autoren bevorzugen die Verwendung des zentralen Zugangs, über den das Gelenkkavum komfortabel ohne Portalwechsel einsehbar ist. Nachteilig ist die potentielle Verletzungsgefahr der tiefen anterioren tibialen neurovaskulären Strukturen.
Das Auffüllen des Gelenks mit 10-20ml physiologischer Kochsalzlösung wird beschrieben, bietet aus Sicht der Autorin aber keinen Vorteil und birgt die Gefahr iatrogener Knorpelverletzungen durch die Punktion mit der Kanüle. Eine Erleichterung der Intubation mit dem Arthroskop wird in ähnlicher Weise erreicht, wenn der Fuß in Neutralstellung positioniert wird, so dass sich die ventralen Kapsel- und Sehnenstrukturen entspannen und gut verschiebbar sind (siehe Video 1). Bei Dorsalextension im Sprunggelenk verschwindet die Knorpelfläche des Talus unter dem Tibiaplafond, was das Risiko von Knorpelverletzungen weiter minimiert.
In manchen Fällen ist die Verwendung von Distraktion hilfreich, um den Talusdom zu erreichen. Hierfür werden verschiedene mechanische Halterungen angeboten. Alternativ kann der Zug mit Hilfe einer Fußschlaufe und eines Gurts, den der Operateur sich um den Körper legt (Abbildung 5) erzeugt werden.
Im Folgenden werden einige ausgewählte OP-Prozeduren an Fallbeispielen veranschaulicht.
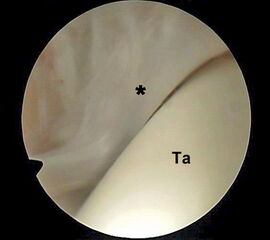
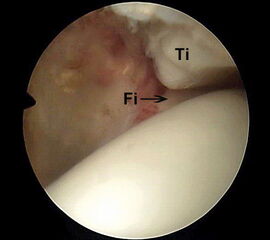
Abbildung 6 und 7, Video 2
Typischer Befund eines fibrotischen Faszikels (*), das zu einem Impingement am rechten lateralen Talus führt. Nach der Resektion des Faszikels ist der Blick auf das anterolaterale Gelenkeck zwischen der Tibia (Ti) und der Fibula (Fi) möglich.
Bei der intraoperativen Palpation mit dem Tasthaken zeigt sich die straffe Spannung des Faszikels und das mechanische Impingement an der lateralen Talusschulter. Oftmals finden sind entzündlich veränderte Synoviaanteile am Faszikel oder auch Schliffspuren am Knorpel der Taluskante.
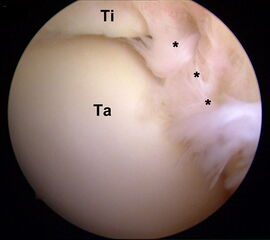
Abbildung 8, Video 3
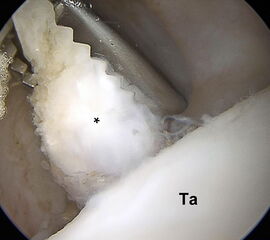
Hypertrophie der Synovia und der Gelenkkapsel (*) im anterolateralen Kompartiment am linken OSG. Das Gewebe rutscht bei Bewegungen und unter Belastung in den Gelenkspalt zwischen Tibia (Ti) und Talus (Ta) und verursacht schmerzhafte Einklemmungen. Es erfolgt eine Resektion mit einer bipolaren Radiofrequenzsonde über das anterolaterale Standardportal. Auf einen ausreichenden Abstand der Radiofrequenzsonde zur Knorpeloberfläche ist zu achten, um iatrogene Hitzeschäden zu vermeiden. Hilfreich ist eine Arbeitsrichtung vom Talushals ausgehend nach kraniolateral. Durch maximale Dorsiflexion des Fußes weitet sich das ventrale Kompartiment und das Gewebe ist weniger gespannt. Hierdurch vergrößert sich der Arbeitsraum und wird die Resektion vereinfacht. Darüber hinaus wird die Knorpeloberfläche des Talus von der Tibia bedeckt und geschützt.
Abbildung 9, Video 4
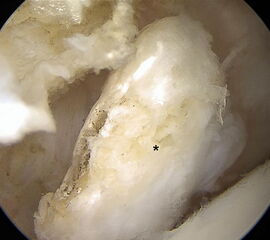
Posttraumatische Arthrofibrose nach bimalleolärer OSG-Fraktur. Die ausgeprägten Verwachsungen (*) erschweren den Zugang zum Gelenk. Oftmals sind die intraartikulären Strukturen und der Gelenkspalt nach dem Einführen des Arthroskops nicht abgrenzbar, so dass zunächst eine Resektion der Narbenstränge mit einem Weichteilshaver erforderlich ist.
Abbildung 10, Video 5
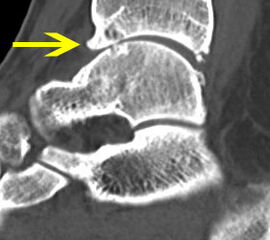
Ventrales knöchernes Impingement durch einen großen Osteophyten an der Tibiavorderkante (Pfeil). Der Osteophyt wird mit einer Kugelfräse (3,5mm Durchmesser) reseziert. Für die Resektion und die abschließende Inspektion sollte in jedem Fall ein Portalwechsel erfolgen, um die vollständige Abtragung sicherzustellen. Gerade bei ausgedehnten osteophytären Anbauten kann es schwierig sein, intraoperativ abzuschätzen, ob ausreichend Knochen reseziert wurde. Hier bietet sich die intraoperative Kontrolle eines Bildverstärkers an. Bilder im seitlichen Strahlengang mit ggf. Innen- und Außenrotation des Sprunggelenks helfen, noch verbliebene Kanten medial und lateral am Sprunggelenk zu lokalisieren.
Abbildung 11 und 12, Video 6
Großer rundlicher Gelenkkörper (*) an der medialen Talusschulter (Ta). Nicht immer liegen diese als Corpora libera vor, sondern sind in der Kapsel oder der Synovia eingebettet und müssen zunächst aus dem Weichteilgeweben gelöst werden, bevor sie mit einer Fasszange extrahiert werden können.
Abbildung 13-14, Video 7
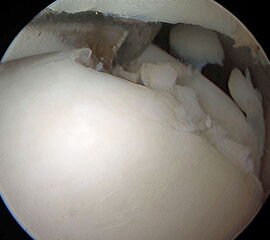
Osteochondrale Läsion an der rechten medialen Talusschulter. Die Knorpelfläche erscheint bei der initialen Inspektion häufig intakt, erweist sich dann bei der Tasthakenpalpation allerdings als deutlich weicher verglichen mit dem umliegenden intakten Knorpelgewebe. In den meisten Fällen lässt sich mit dem Tasthaken ein Riss in der Oberfläche nachweisen und eine lose chondrale bzw. osteochondrale Schuppe abheben. Die instabilen Knorpelanteile und die sklerotisch veränderten Anteile der subchondralen Knochenschicht müssen mit einer Kürette oder einem Shaver entfernt werden, bis ein stabiler Rand aus gesundem Knorpelgewebe besteht. Die Eröffnung des subchondralen Knochens erfolgt mit einer gebogenen Ahle. Anschließend (ggf. nach dem Öffnen der Blutsperre) sollten kleine Blutungen aus den Knochenkanälen erkennbar sein.
Video 8
Alternativ kann zur Knochenmarkstimulation eine Anbohrung der Läsion mit einem dünnen K-Draht durchgeführt werden (in Abhängigkeit von der Größe der Läsion 1,0-2,0mm K-Draht).
Postoperative Behandlung
Das postoperative Nachbehandlungsregime richtet sich nach dem durchgeführten Eingriff.
Synovialektomie, Weichteildebridement, Arthroylse, Entfernung freier Gelenkkörper, Osteophytenresektion:
- Teilbelastung mit 20kg an Unterarmgehstützen für 3-5 Tage postoperativ je nach Schwellungszustand, dann Übergang zur Vollbelastung bei reizlosen Wundverhältnissen.
- Bei Resektion von Osteophyten oder Entfernung von Gelenkkörpern postoperative Röntgenkontrolle des OSG.
- Entfernen der Hautfäden nach 12-14 Tagen.
- Passive und aktive Physiotherapie ab dem 1. postoperativen Tag (freier Bewegungsumfang), bedarfsweise manuelle Lymphdrainage.
- Nach einer Arthrolyse Verordnung einer CPM (continuous passive motion)-Bewegungsschiene für das Sprunggelenk.
- Sportpause für 3-4 Wochen postoperativ.
Knochenmarkstimulierende Verfahren (Mikrofrakturierung, Pride-Bohrung, retrograde Anbohrung), Refixation osteochondraler Flakes, retrograde Auffüllung subchondraler Zysten:
- Teilbelastung mit 20kg an Unterarmgehstützen für 6 Wochen postoperativ.
- Bei Refixation osteochondraler Flakes und Zystenauffüllung postoperative Röntgen- oder CT-Kontrolle des OSG.
- Entfernen der Hautfäden nach 12-14 Tagen.
- Passive und aktive Physiotherapie ab dem 1. postoperativen Tag (freier Bewegungsumfang), bedarfsweise manuelle Lymphdrainage.
- Ggf. Verordnung einer CPM (continuous passive motion)-Bewegungsschiene für das Sprunggelenk.
- Sportpause für 3 Monate postoperativ, keine Pivoting-Sportarten für 6 Monate 6.
Arthroskopische Frakturversorgung und OSG-Arthrodese:
- Teilbelastung mit 20kg an Unterarmgehstützen für 6-8 Wochen postoperativ. Weiterer Belastungsaufbau nach Röntgenkontrolle.
- Walkerorthese für 6-8 Wochen postoperativ. Anschließend bei Arthrodesen je nach Röntgenbefund noch für weitere 2-3 Monate Versorgung mit einem hochschaftigen, konfektionierten Stiefel (z.B. Orthotech Variostabil Stiefel™, Künzli Ortho® Stabilschuh) mit stufenweisem Belastungsaufbau. Nach vollständiger Überbauung Versorgung im Konfektionsschuh mit Abrollhilfe.
- Postoperative Röntgen- oder CT-Kontrolle des OSG.
- Entfernen der Hautfäden nach 12-14 Tagen.
- Physiotherapie in Abhängigkeit von der Stabilität des gewählten Osteosyntheseverfahrens, bedarfsweise manuelle Lymphdrainage.
Fehler, Gefahren, Komplikationen
- Verletzung der Tibialis anterior-/Extensor hallucis longus-/Extensor digitorum longus-Sehne: dies kann vermieden werden, indem das obere Sprunggelenk bei der Operation in Neutralstellung gehalten wird. In dieser Position sind die ventral verlaufenden Strukturen weniger unter Spannung und können den penetrierenden Instrumenten besser ausweichen. Hilfreich ist das Einzeichnen des Verlaufs der anatomischen Strukturen auf der Haut. Bei der Anlage der Portale sollte lediglich die Haut mit dem Skalpell vorsichtig inzidiert und die tiefer gelegenen Weichteile mit einem Klemmchen stumpf aufgespreizt werden. Um eine Verletzung der ventral verlaufenden Strukturen zu verhindern, sollte das ventrale Weichteildebridement möglichst sparsam durchgeführt, es gilt: so wenig wie möglich, so viel wie nötig! Durch die Dorsiflexion im Sprunggelenk weitet sich der ventrale Gelenkraum 7, so dass deutlich weniger Weichteilgewebe reseziert werden muss, um gute Sichtverhältnisse auf das Gelenk zu erlangen (siehe unten). Die Öffnung des Shavers und der HF-Sonde sollten nicht nach ventral ausgerichtet werden.
- Verletzung des anterioren tibialen Gefäßnervenbündels/Pseudoaneurysmen: siehe oben. Das Risiko einer Verletzung der Vasa tibialis anterior besteht vor allem bei der Verwendung des anterozentralen Portals. In der Regel ermöglichen das anteromediale und anterolaterale Standardportal eine vollständige Inspektion und Adressierung von Pathologien im ventralen Kompartiment, so dass auf eine zusätzliche Anlage eines anterozentralen Zugangs meist verzichtet werden kann.
- Läsion der N. Äste des N. peroneus superficialis (N. cutaneus dorsalis medialis et intermedius): siehe oben. Der N. cutaneus dorsalis medialis ist bei schlanken Patienten bei forcierter Plantarflexions- und Inversionsstellung des Fußes oftmals gut unter Haut zu palpieren. Befindet sich das Arthroskop bereits über das anteromediale Portal im Gelenk, kann durch die Ausrichtung der Lichtquelle nach ventral der Verlauf der Nerven mittels Diaphanoskopie dargestellt werden. Ein erhöhtes Verletzungsrisiko besteht vor allem bei posttraumatischen Situationen mit ausgedehnten Vernarbungen im Gelenk und eingeschränkten Sichtverhältnissen.
- Traktionsbedingte Schäden: die Traktion sollte sukzessive und wohl dosiert eingesetzt werden. Wird ein mechanischer Distraktor verwendet, muss die Weichteilspannung der extraartikulären Strukturen nach Anlage des Zugs unbedingt überprüft werden. Sanfter und besser steuerbar ist die Erweiterung des Gelenkspalts durch das eigene Körpergewicht des Operateurs über ein Gurtsystem (siehe Abbildung 5). Invasive Distraktoren mit Steinmannpins werden aufgrund der erhöhten Komplikationsrate kaum noch verwendet.
- Kompartmentsyndrom: hierbei handelt es sich um eine äußerst seltene Komplikation, die durch eine Kompression der neurovaskulären Strukturen infolge einer Weichteilschwellung verursacht wird. Um ein Anschwellen der Weichteile zu verhindern, sollte der Pumpendruck bei der OSG-Arthroskopie nicht höher als 30-50mmHg liegen. Eine exzessive Resektion der Gelenkkapsel begünstigt das Austreten von Arthroskopieflüssigkeit ins Gewebe und sollte daher vermieden werden.
- Iatrogene Knorpelschäden: aufgrund der extrem kongruenten Form und der straffen ossären und ligamentären Führung ist der Gelenkraum für das arthroskopische Vorgehen eng. Vorteilhaft ist deswegen die Verwendung einer kurzen, dünnen Optik (z.B. 2,7 mm Durchmesser) und spezieller Instrumente für die OSG-Arthroskopie. Beim Einführen des Arthroskopieschaftes sollte ein stumpfer Trokar oder der Wechselstab verwendet werden. Intraoperativ sollten die Instrumente stets unter arthroskopischer Sicht eingesetzt werden. Durch eine Dorsiflexion des Fußes wird die ventrale Kapsel entspannt, was in einer Ausweitung des Arbeitsraums mit verbesserten Sichtverhältnissen und vereinfachtem Instrumentenmanagement resultiert. Darüber hinaus wird die Knorpeloberfläche des Talus durch die Tibia geschützt (siehe Video 3).
- Verbliebene Osteophytenreste oder Gelenkkörper: durch den Vergrößerungseffekt des Arthroskops kann es zu Fehleinschätzungen des Resektionsausmaßes kommen. Darüber hinaus können Knochenfragmente im Weichteilgewebe übersehen werden. Dies kann durch die intraoperative Kontrolle mit dem Bildverstärker vermieden werden. Osteophyten und Gelenkkörper können ggf. unter Durchleuchtungskontrolle mit einer Kanüle markiert werden, um sie leichter im Weichteilgewebe zu identifizieren.
- Wundheilungsstörungen/Fistelbildung: das Risiko einer Wundheilungsstörung oder Fistelbildung kann durch einen suffizienten Wundverschluss deutlich reduziert werden. Die Portale sollten anstelle von Klammerpflastern o. ä. mittels Einzelknopf- oder Einzelknopfrückstichnähte verschlossen werden. Bewährt haben sich 2 Nähte pro Portal, um die Haut fest zu adaptieren. Eine Teilbelastung des Fußes sollte mindestens eingehalten werden, bis die Wundsekretion sistiert.
Die Komplikationsrate in der Sprunggelenksarthroskopie wurde in den 80er Jahren mit 13,6-24,6% sehr hoch beziffert. Dies lag vor allem an der Anwendung großer, für die OSG-Arthroskopie ungeeigneter Instrumente und an dem Einsatz invasiver Distraktoren (Sprague 1989). In der Literatur bis zum Jahr 2000 wird eine durchschnittliche Komplikationsrate von 10,3% angegeben. Davon entfallen 3,7% auf Nervenläsionen 89101112131415. Bei genauer Analyse der Daten zeigt sich allerdings, dass es sich überwiegend um transiente Läsionen im Sinne einer Neurapraxie handelt. Zengerink und van Dijk konnten 2012 in ihrem eigenen Patientengut bei insgesamt 1305 Eingriffen eine deutlich niedrigere Komplikationsrate von insgesamt nur 3,5% nachweisen 16. Die Autoren führen dies auf die konsequente Durchführung der oben beschriebenen Maßnahmen wie Dorsiflexion des Fußes, Inzision der Haut mit anschließend stumpfer Präparation des Portals, korrekte Ausrichtung der Instrumente, sowie dosierte, intermittierende Anwendung der Distraktion zurück. Ähnliche Angaben finden in sich in einer Metaanalyse von Simonson und Roukis 17. Bei der durchschnittlichen Gesamtkomplikationsrate der OSG-Arthroskopie von 4% handelte es sich 3,2% der Fälle um sog. Minorkomplikationen. Lediglich 0,8% wurden als Majorkomplikationen eingestuft.
Ergebnisse
Die Darstellung der Ergebnisse der arthroskopischen Behandlung einzelner Pathologien am OSG erweist sich als schwierig, da oftmals kombinierte Veränderungen vorliegen. Das ossäre Impingement tritt meist in Kombination mit einem Weichteilimpingement auf 18. Darüber hinaus sind chronische chondrale bzw. osteochondrale Läsionen ebenfalls häufig mit einer einklemmenden Weichteilhypertrophie assoziiert.
Für das isolierte weichteilbedingte OSG-Impingement werden 84-94% sehr gute und gute klinische Resultate beschrieben 19202122. Hassan wies bei 23 Patienten nach einem Follow-up von durchschnittlich 25 Monaten eine Verbesserung des AOFAS Scores von 34 (Range 4-57) auf 89 (Range 60-100) nach 23. Ebenfalls sehr gute Ergebnisse erzielten Gulish et al. bei ihren Patienten mit einem postoperativen AOFAS Score von 95 24 sowie Koczy et al. mit einer Steigerung von 75,4 auf 92 Punkte im AOFAS Score 12 Monate nach dem Eingriff 25.
Die erste und bis dato einzige Untersuchung zur arthroskopischen Behandlung des isolierten anterioren knöchernen Impingementsyndroms wurde 1993 von Ogilvie-Harris et al. publiziert. Bei 16 von 17 Patienten wurde eine signifikante Verbesserung der Schwellung, des Schmerzlevels und der Dorsiflexion im OSG erreicht 26. In den meisten Fällen des ventralen Sprunggelenkimpingements wird die arthroskopische Osteophytenabtragung mit einer Synovialektomie kombiniert. Dies liefert ähnlich gute Resultate wie das isolierte Weichteildebridement. Rasmussen berichtet über 89% exzellente und gute Ergebnisse bei kombiniertem Vorgehen 27. Bauer et al. erzielten in ihrer Nachuntersuchung eine signifikante Verbesserung der Dorsiflexion von 7° auf 16° und in der Plantarflexion von 20° auf 34° nach einer ausgedehnten anterioren Synovialektomie mit Osteophytenresektion 28. Die Autoren betonen die Wichtigkeit der frühzeitigen und intensiven Mobilisation und Bewegungstherapie zum Erhalt des intraoperativ erreichten Bewegungsumfangs. In der Studie von Murawski und Kennedy wurde eine Steigerung von 62,83 auf 91,17 Punkte im AOFAS Score sowie eine Verbesserung von 61,54 auf 92,21 Punkte im SF 36v2 Score nachgewiesen 29. 93% der Betroffenen waren mit dem Ergebnis sehr zufrieden und 40 der 41 Patienten (97,5%) erreichten ihren präoperativen sportlichen Aktivitätslevel.
In wie fern sich begleitende Pathologien auf das Ergebnis der arthroskopischen Therapie des anterioren OSG-Impingements auswirken ist umstritten. In der Studie von Mardani-Kivi et al. hatte das das Vorliegen eines chondralen Schadens keinen Einfluss auf das postoperativen Ergebnisse 30. Parma et al. hingegen wiesen einen signifikanten Zusammenhang zwischen dem klinischen Ergebnis nach OP und der Schwere des begleitenden Knorpelschadens nach 31.
Der Übergang vom Impingementsyndrom durch Osteophyten mit lokalen degenerativen Veränderungen zur generalisierten Arthrose ist fließend. Der Nutzen der Arthroskopie bei Gelenkverschleiß wird kontrovers diskutiert. Am oberen Sprunggelenk wurde gezeigt, dass bei generalisierten degenerativen Veränderungen nur 62% der Patienten über eine Besserung der Schmerzsymptomatik nach dem arthroskopischen Eingriff berichten. Eine normale Gelenkfunktion ließ sich nur in 7% der Fälle wiederherstellen 32. Offensichtlich profitieren lediglich Patienten mit einer lokalisierten Arthrose von einer Synovialektomie mit Osteophytenresektion und Knorpelglättung 233, (Lampert 2011). Weniger entscheidend für den Behandlungserfolg ist die Größe und Lokalisation der Osteophyten als die präoperativ bestehende Gelenkspaltverschmälerung. In einer Untersuchung von Tol et al. ließen sich bei Patienten mit einer reduzierten Gelenkspalthöhe in nur 53% der Fälle gute und exzellente postoperative Scores erzielen, wohingegen bei den Patienten ohne Gelenkspaltverschmälerung die Rate bei 77% lag 18. Aus derselben Arbeitsgruppe liegt eine weitere Studie vor mit der Verteilung 73% vs. 90% exzellente/gute Ergebnisse (van Dijk 2014). Daraus wird gefolgert, dass der Benefit des Debridements am arthrotischen OSG bei einer Gelenkspaltweite < 2mm deutlich limitiert ist (Lampert 2011).
Bei den chondralen und osteochondralen Schäden müssen die akuten Verletzungen im Sinne einer Flake Fraktur von den chronischen Läsionen differenziert werden. Bei den chronischen Veränderungen ist ein Refixationsverfahren aufgrund der schlechten Heilungskapazität des meist avitalen Dissekats wenig erfolgversprechend. Für die arthroskopischen knochenmarkstimulierenden Techniken wie Pridie-Bohrung und Mikrofrakturierung werden in der Literatur gute Ergebnisse beschrieben 34353637383940414243644. Zengerink et al. haben die Daten von insgesamt 386 Patienten aus 18 Studien zusammengefasst und stellten eine Erfolgsrate von 85% fest 45. Diese liegt deutlich höher als bei der alleinigen Exzision des Dissektats (durchschnittliche Erfolgsrate 54%) und der Exzision in Kombination mit einer Kürettage (durchschnittliche Erfolgsrate 77%) (van Dijk 2014). Da die arthroskopische Knochenmarkstimulation (KMS) ähnlich gute Resultate wie der autologe osteochondrale Knorpelknochentransfer (OATS) (87%) und bessere Resultate als die autologe Chondrozytentransplantation (76%), aber deutlich kostengünstiger und weniger invasiv ist, empfehlen die Autoren die arthroskopische antegrade KMS als Primärtherapie 45. Die Grenze der Defektgröße für ein erfolgreiches Ergebnis nach einer Mikrofrakturierung wird mit 1,5cm² angegeben 4647. Größere Defektausmaße, präoperativ länger bestehende Symptomdauer sowie ein erhöhter Body Mass Index beeinflussen das Ergebnis tendenziell negativ 46474849. Das Patientenalter hingegen scheint keine Auswirkung auf den Therapieerfolg der Knochenmarkstimulation zu haben 4849505152.
Bei der frischen traumatischen Verletzungen werden die chondralen Abscherungen von den osteochondralen Frakturen unterschieden. Die Fixation einer Knorpelschuppe ist aufgrund der mangelhaften Anheilung nicht sinnvoll. In diesen Fällen bleibt nur die Entfernung des Fragments. Hinsichtlich der Indikation zur Fixation eines osteochondralen Flakes existieren keine evidenzbasierten Richtlinien. Gemäß der aktuellen Datenlage wird eine Refixierung bei Fragmenten mit einem Durchmesser >15 mm bei ausreichender spongiöser Substanz an der Unterseite des Fragments empfohlen 1, (van Dijk 2014).
In den vergangenen 25 Jahren wurde eine Vielzahl retrospektiver klinischer Studien zu den Ergebnissen nach arthroskopischer OSG-Arthrodese veröffentlicht. Die erste Arbeit, in der die Resultate der arthroskopischen mit der offenen Arthrodese verglichen werden, wurde 1991 von Myerson und Quill publiziert 53. Sowohl der Zeitraum der radiologisch nachgewiesenen knöchernen Fusion (8,7 vs. 14,5 Wochen) als auch die Dauer des Krankenhausaufenthaltes (1,5 vs. 4 Tage) waren im arthroskopisch behandelten Kollektiv kürzer. Bei der arthroskopischen Gelenkversteifung zeigte sich eine höhere Fusionsrate (100% vs. 94,1%). Neuere Vergleichsstudien kommen zu sehr ähnlichen Ergebnissen 5455. Fasst man die Daten der vorliegenden Nachuntersuchungen zusammen, liegt die Fusionsrate der arthroskopischen Arthrodese am oberen Sprunggelenk bei 89-100% 356575859606162636465. Gute und exzellente Resultate mit einer hohen Patientenzufriedenheit werden in 80-100% der Fälle berichtet 35664. Als weitere Vorteile sind der kürzere Zeitraum bis zur knöchernen Durchbauung der Arthrodese 56606463 und die schnellere Rehabilitation zu nennen.
Weitere Literatur
- Tagaki K. The arthroscope. J Jpn Orthop Assoc 1939; 14: 359.
- Watanabe M. Selfoc-Arthroscope (Watanabe No. 24 Arthroscope monography). Tokyo, Teishin Hospital, 1972.
- Chen YC. Clinical and cadaver studies on the ankle joint arthroscopy. J Jpn Orthop Assoc 1976; 50: 631-51.
- Hempfling H. Arthroskopie des oberen Sprunggelenks. Trauma Berufskrankh 2001; 3: 326-32.
- Lampert C. Arthroskopie bei Arthrose des oberen Sprungelenks. Arthroskopie 2011; 24: 262-67.
- Van Dijk CN, Kennedy J (eds). Talar Osteochondral Lesions. Diagnosis, Planning, Treatment and Rehabilitation. Heidelberg, New York, Dordrecht, London: Springer, 2014.
- Sprague NF III, Guhl JF, Olson DW. Specific complications: elbow, wrist, hip, and ankle. In: Sprague NF III (ed). Complication in arthroscopy. New York: Raven Press, 1989.